��Ŀ����
��15�֣��Ը������������Ĺ�ҵ��ҺΪԭ�������������Ĺ������£����ֲ����������ԣ���
I �ӷ�Һ���ᴿ���ᾧ��FeSO4?7H2O��
II��![]() ��Һ���Թ�����
��Һ���Թ�����![]() ��Һ��ϣ��õ���
��Һ��ϣ��õ���![]() ����Һ
����Һ
IV ����Һ���ˣ���90��C��ˮϴ�ӳ����������õ�![]() ����
����
V����![]() ���õ�
���õ�![]() ����
����
��֪��![]() ����ˮ�зֽ�
����ˮ�зֽ�
��1�� I�У�����������м��ȥ��Һ�е�![]() ���÷�Ӧ�����ӷ���ʽ��
���÷�Ӧ�����ӷ���ʽ��
��2�� II�У����һ�������ᣬ���û�ѧƽ��ԭ���������������
��3�� III�У�����![]() �����ӷ���ʽ�� ����
�����ӷ���ʽ�� ����![]() ��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ���ñ仯�Ļ�ѧ����ʽ�� ��
��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ���ñ仯�Ļ�ѧ����ʽ�� ��
��4�� IV�У�ͨ������![]() ���жϳ����Ƿ�ϴ�Ӹɾ�������
���жϳ����Ƿ�ϴ�Ӹɾ�������![]() �������� ��
�������� ��
��5�� ��֪����![]() �Ļ�ѧ����ʽ��
�Ļ�ѧ����ʽ��![]() ��������
��������
464.0kg��![]() ���õ�316.8kg��Ʒ������Ʒ������ֻ��
���õ�316.8kg��Ʒ������Ʒ������ֻ��![]() ����ò�Ʒ��
����ò�Ʒ��![]() �������� kg��Ħ������/g?
�������� kg��Ħ������/g?![]() ��
��![]() ��
��
![]() (1)Fe + 2Fe3+ = 3Fe2+
(1)Fe + 2Fe3+ = 3Fe2+
(2)�������ᣬH+Ũ������ʹFe2+ + 2H2O![]() Fe(OH)2 + 2H+��ƽ�����淴Ӧ�����ƶ����Ӷ�����FeSO4��ˮ��
Fe(OH)2 + 2H+��ƽ�����淴Ӧ�����ƶ����Ӷ�����FeSO4��ˮ��
![]()
![]() ��3��Fe2+ + 2HCO3- = FeCO3��+ CO2 �� + H2O
��3��Fe2+ + 2HCO3- = FeCO3��+ CO2 �� + H2O
![]()
![]() 4FeCO3 + 6H2O + O2 = 4Fe(OH)3 ��+ 4CO2
4FeCO3 + 6H2O + O2 = 4Fe(OH)3 ��+ 4CO2
![]()
![]() ��4��ȡ����ϴ�Ӻ����Һ�����Թ��У��μ��ữ��BaCl2��Һ�����ް�ɫ���������������ϴ�Ӹɾ�
��4��ȡ����ϴ�Ӻ����Һ�����Թ��У��μ��ữ��BaCl2��Һ�����ް�ɫ���������������ϴ�Ӹɾ�
![]()
![]() ��5��288.0
��5��288.0
![]() ���������⿼�黯ѧʵ��������������ʵ��Ʊ�����ѧ��Ӧԭ��������ȡ���1��Fe3�����������ԣ�������Fe����Fe2����2Fe3�� + Fe��3Fe2����
���������⿼�黯ѧʵ��������������ʵ��Ʊ�����ѧ��Ӧԭ��������ȡ���1��Fe3�����������ԣ�������Fe����Fe2����2Fe3�� + Fe��3Fe2����
��2������Fe2��ˮ�⣬����H2SO4����ֹ��ˮ�⡣
��3��Fe2����HCO3����Һ�з���˫ˮ������FeCO3��Fe2�� + 2HCO3��FeCO3��+ CO2��+ H2O��FeCO3�ڱ�O2������������Fe(OH)3�����ֺ��ɫ��4FeCO3 + O2 + H2O��Fe(OH)3 ��+ 4CO2����
��4��SO42�ļ���һ�����BaCl2��Һ��������Һ��BaCl2��Һ��Ӧ�Ƿ��а�ɫ�����������ж���Һ���Ƿ����SO42��
��5��464kg FeCO3�к���FeԪ��4��103mol�����Ʒ��FeO xmol ��Fe2O3ymol�����У�x + 2y��4��103��72x + 160y��316.8��103�����x��2.2��103mol��y��1.8��103mol����Fe2O3��������1.8��103mol��160g/mol��288.0kg��

 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� ����
����
 I �ӷ�Һ���ᴿ���ᾧ��FeSO4��7H2O��
I �ӷ�Һ���ᴿ���ᾧ��FeSO4��7H2O�� ��Һ���Թ�����
��Һ���Թ����� ��Һ��ϣ��õ���
��Һ��ϣ��õ��� ����Һ
����Һ IV ����Һ���ˣ���90��C��ˮϴ�ӳ����������õ�
IV ����Һ���ˣ���90��C��ˮϴ�ӳ����������õ�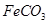 ����
���� ����
����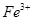 ���÷�Ӧ�����ӷ���ʽ��
���÷�Ӧ�����ӷ���ʽ��
 ���жϳ����Ƿ�ϴ�Ӹɾ�������
���жϳ����Ƿ�ϴ�Ӹɾ������� ��֪����
��֪���� ��������464.0kg��
��������464.0kg�� ����ò�Ʒ��
����ò�Ʒ�� ��������
kg��Ħ������/g��
��������
kg��Ħ������/g�� ��
�� ��
��