题目内容
在一个密闭容器中,可逆反应aA(g)==bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向正反应方向移动了 B.物质A的转化率减小了
C.物质B的质量分数增加了 D.a>b
AC。
错解分析:没有真正理解量的变化(体积变化引起浓度变化)关系。根据题意,当体积增大时,B的浓度减小,因此。增大体积(减小压强)时平衡向左移动,因此A的转化率减小。根据平衡移动原理,可知a>b。错选BD。
解题指导:当容器的体积增大一倍时,若平衡不发生移动,B的浓度应该为原来的50%。但题目指出,新平衡中B的浓度为原来的60%(大于50%),因此说明平衡发生移动,而且朝正反应方向移动。

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
在一个密闭容器中有可逆反应:A+2B(g)?3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系.根据上述图象判断下列说法错误的是( )
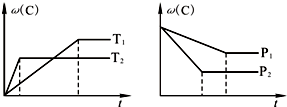

| A、T1<T2,该可逆反应的正反应为放热反应 | B、P1<P2,A为非气态物质 | C、达到平衡时,再加入少量反应物A,可使反应物B的转化率增大 | D、恒容条件下混合气体的密度保持不变时反应一定达到平衡 |
 在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分.当左边充入28gN2,右边充入8gCO和CO2的混合气体时,隔板处于如图所示位置(两侧温度相同).则混合气体中CO和CO2的分子个数比为( )
在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分.当左边充入28gN2,右边充入8gCO和CO2的混合气体时,隔板处于如图所示位置(两侧温度相同).则混合气体中CO和CO2的分子个数比为( )
 3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系。根据上述图象判断下列说法错误的是
3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系。根据上述图象判断下列说法错误的是 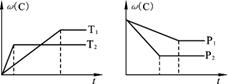
 2NH3 。
2NH3 。