题目内容
用合适的漏筛可以除去大米中的细沙,其原理与下列哪种分离物质的方法相同? ( )
| A.洗涤 | B.萃取 | C.过滤 | D.蒸馏 |
C
解析试题分析:A、在洗涤时,通过一些化学物质(如洗涤剂等)的作用以减弱或消除污垢与载体之间的相互作用,使污垢与载体的结合转变为污垢与洗涤剂的结合,最终使污垢与载体脱离,错误;B、萃取是利用系统中组分在溶剂中有不同的溶解度来分离混合物的单元操作,错误;C、过滤是指在推动力或者其他外力作用下悬浮液(或含固体颗粒发热气体)中的液体(或气体)透过介质,固体颗粒及其他物质被过滤介质截留,从而使固体及其他物质与液体(或气体)分离的操作,正确;D、蒸馏是一种热力学的分离工艺,它利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的单元操作过程,是蒸发和冷凝两种单元操作的联合,错误。
考点:分离物质的方法。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
可以用分液漏斗分离的一组液体混合物是( )
| A.溴和四氯化碳 | B.苯和溴苯 | C.汽油和苯 | D.硝基苯和水 |
下列提纯物质方法正确的是
| A.用BaCl2溶液除去HNO3溶液中的少量H2SO4 |
| B.用NaOH溶液除去铝粉中的少量铁粉 |
| C.用氯水除去FeCl2溶液中的少量FeCl3 |
| D.用加热法除去NaCl固体中的少量NH4Cl |
以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
| A.加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液中一定含NH4+ |
| B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定有大量的CO32- |
| C.用洁净的铂丝蘸取待测溶液,置于火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色。该溶液中一定含有钾离子,可能含有钠离子 |
| D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl- |
下列实验设计和结论正确的是( )
| A.向某溶液中加入盐酸后产生能使澄清石灰水变浑浊的无色无味气体,则该溶液一定含有CO32- |
| B.向饱和Na2CO3溶液中通入足量的CO2后溶液变浑浊,是因为析出了NaHCO3晶体 |
| C.向某溶液中加入适量新制氯水和几滴KSCN溶液后呈红色,则该溶液一定含有Fe2+ |
| D.向某溶液中滴加BaCl2溶液后产生不溶于稀硝酸的白色沉淀,则该溶液一定含有Ag+ |
用下列实验装置进行相应实验,能达到实验目的的是
| A.用图1 所示装置除去Fe(OH)3胶体中含有的少量FeCl3杂质 |
| B.用图2 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3 所示装置从海水制取蒸馏水 |
| D.用图4 所示装置分离酒精萃取碘水中的碘 |
下列实验中,所选装置不合理的是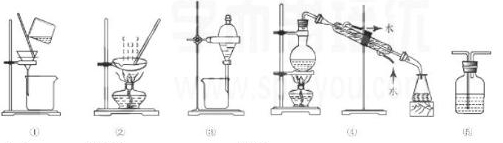
| A.分离Na2CO3溶液和CCl4,选④ |
| B.用CC14提取碘水中的碘,选③ |
| C.用FeC12溶液吸收C12,选⑤ |
| D.粗盐提纯,选①和② |
粗盐提纯实验用到的试剂中,不是为了除去原溶液中杂质离子的是( )
| A.盐酸 | B.烧碱溶液 | C.纯碱溶液 | D.氯化钡溶液 |