题目内容
下列说法正确的是
A.把100mL3mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度改变为1.5mol·L-1
B.把100g20%的NaCl溶液跟100gH2O混合后,NaCl溶液的质量分数是10%
C.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后,溶液中的C(Cl-)仍然是3mol·L-1
D.把100mL20%的NaOH溶液跟100mLH2O混合后,NaOH溶液的质量分数是10%
B
解析:
A错,因为100mL3mol·L-1的H2SO4跟100mLH2O混合后的体积小于200Ml;
B正确,ω=100×20%/(100+100)=10%;C错,因为3mol·L-1的BaCl2溶液中的氯离子浓度为6mol·L-1,混合后溶液中氯离子浓度大于3mol·L-1;D错,因为NaOH溶液的密度大于1g/Ml,
加入水的质量等于100g,所以混合后溶液中溶质的质量大于10%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

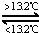 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,