题目内容
一包白色粉末,由几种常见的盐混合组成,其中只可能含有Na+、K+、Al3+、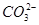 、
、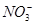 、
、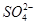 、
、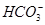 、
、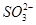 中的若干种离子。某同学对该溶液进行如下实验:
中的若干种离子。某同学对该溶液进行如下实验:
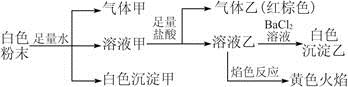
以下说法正确的是
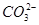 、
、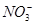 、
、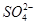 、
、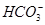 、
、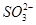 中的若干种离子。某同学对该溶液进行如下实验:
中的若干种离子。某同学对该溶液进行如下实验:
以下说法正确的是
A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和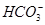 |
| B.气体乙一定是NO和NO2的混合气体 |
C.白色沉淀乙是BaSO4,所以原混合物一定含有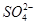 |
| D.焰色反应为黄色火焰,不能确定原混合物中不含K+ |
D
由混合物中所含离子看出,白色沉淀只能是Al(OH)3,为Al3+和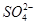 或Al3+和
或Al3+和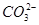 发生相互促进的水解反应而得,只能说明含
发生相互促进的水解反应而得,只能说明含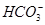 和
和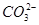 中的至少一种,不能确定是否含有
中的至少一种,不能确定是否含有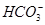 ,A项错误;气体乙中可能含CO2或SO2,B项错误;白色沉淀乙为BaSO4,乙中
,A项错误;气体乙中可能含CO2或SO2,B项错误;白色沉淀乙为BaSO4,乙中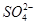 也可能是
也可能是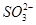 被NO在酸性条件下氧化的结果,C项错误。只有D项正确。
被NO在酸性条件下氧化的结果,C项错误。只有D项正确。
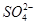 或Al3+和
或Al3+和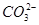 发生相互促进的水解反应而得,只能说明含
发生相互促进的水解反应而得,只能说明含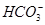 和
和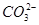 中的至少一种,不能确定是否含有
中的至少一种,不能确定是否含有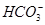 ,A项错误;气体乙中可能含CO2或SO2,B项错误;白色沉淀乙为BaSO4,乙中
,A项错误;气体乙中可能含CO2或SO2,B项错误;白色沉淀乙为BaSO4,乙中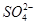 也可能是
也可能是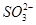 被NO在酸性条件下氧化的结果,C项错误。只有D项正确。
被NO在酸性条件下氧化的结果,C项错误。只有D项正确。
练习册系列答案
相关题目
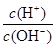 =1012的溶液:Fe2+、Mg2+、NO3-、Cl-
=1012的溶液:Fe2+、Mg2+、NO3-、Cl-
 H2CO3 H2CO3
H2CO3 H2CO3 、
、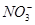 、Na+
、Na+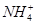 、
、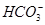 、
、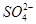 、
、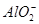
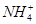 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、 、
、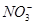 、
、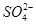 ,已知:
,已知: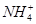 )由大到小的顺序为________;
)由大到小的顺序为________;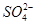 。该溶液中c(H+)_________________________c(OH-)+c(
。该溶液中c(H+)_________________________c(OH-)+c(