��Ŀ����
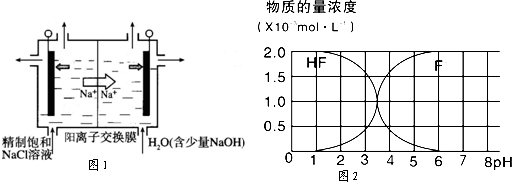
�������ȣ�ClO2����һ�ֹ��ס���Ч��ɱ���������������������Ƶ�ǿ�Ҵ̼�����ζ��������ˮ���е�11�棬���Ȳ��ȶ��ֽⷢ����ը��һ�ֹ�ҵ�Ʒ���������(��Ҫ�ɷ�ΪFeS2)��ԭ��������ȡ�������ȣ�ij�о�С����ʵ�����������װ���Ʊ�ClO2��ˮ��Һ��
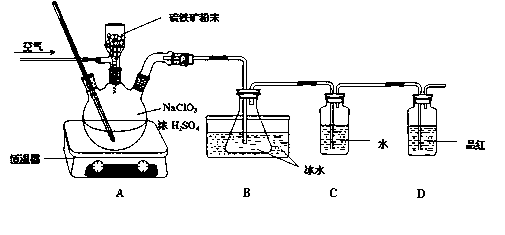
��1��������ƿ�м���NaClO3��Һ��ŨH2SO4��ͨ����������ں�������60�棬ͨ������������������ټ����������ĩ����Ӧ��ʼʱ��ƿ�ڷ�����Ӧ�����ӷ���ʽ���£�����ƽ�÷���ʽ����ClO3�� ����FeS2����H������ClO2����Fe3������SO42������H2O
��2��װ��D�������� ��
��3����������Ӧ���ķ�Һ(�����������⣬����Al3����Mg2����H����Cl����)���Ʊ�Ħ���Σ���(NH4)2Fe(SO4)2��6H2O��������������£�
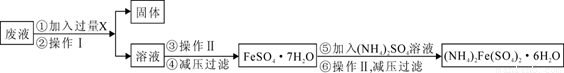
�ش��������⣺
�ٲ����������Ϊ�� ��
���Լ�X�� ��д����������Ҫ��Ӧ�����ӷ���ʽ ��
��Ϊ�ⶨ(NH4)2Fe(SO4)2��6H2O���������ĺ�����ijʵ��С����������ʵ�飺�õ�����ƽȷ����5.000g��������茶��壬���Ƴ�250mL��Һ��ȡ������Һ25.00mL����ƿ�У���ϡH2SO4�ữ����0.01000mol/L KMnO4��Һ�ζ���Fe2+ǡ��ȫ��������Fe3+��ͬʱ��MnO4������ԭ��Mn2+���������KMnO4��Һ��ƽ�����Ϊ21.00mL����þ�����������������Ϊ ��������4λ��Ч���֣�
��1��15ClO3�� �� FeS2�� 14H���� 15ClO2�� Fe3����2SO42����7H2O ��3�֣�
��2������ClO2�Ƿ�������ȫ��2�֣�
��3���ٹ��ˣ�2�֣� ��Fe��2�֣��� 2Fe3����Fe��3Fe2����2�֣�����11.76%��3�֣�
��������
�����������1����ƽʱ��������Ԫ���ǰ���1�s2���еģ��ܹ�ʧȥʮ��Ħ���ĵ��ӣ�����Ԫ���ܹ��õ�һĦ���ĵ��ӣ���������������ǰ�����ʮ�壬Ȼ����غ㣬�������غ��������������Ϳ��Եõ����¹�ϵʽ��15ClO3�� �� FeS2�� 14H���� 15ClO2�� Fe3����2SO42����7H2O ��3�֣�
��2����Ϊ�������ȣ�ClO2����һ�ֹ��ס���Ч��ɱ������������һ������ǿ�ҵ������ԣ�����û�б�������Ļ������뵽����Dƿ�У�����ʹƷ����ɫ����������������ClO2�Ƿ�������ȫ�ģ�2�֣�
��3����һ������Ҫ�ù������������ɵ����������ӻ�ԭΪ���ۣ���ˢٵIJ����ǹ��ˣ�2�֣� ��Fe��2�֣��� 2Fe3����Fe��3Fe2����2�֣���
�ۼ��������ӵ����ʵ���Ϊxmol
MnO4�� �� �� �� 5Fe2+
1mol 5mol
0.01000mol/L��21.00mL��10 x
��֮�ã�x��1.05��10��2mol,��������������Ϊ��
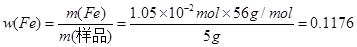 =11.76%
=11.76%
���㣺������ƽ����ʽ�Լ��������ȵ������ԡ�

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д� ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д� �������ȣ�ClO2��Ϊһ�ֻ���ɫ���壬�ǹ����Ϲ��ϵĸ�Ч�����ס����١���ȫ��ɱ����������
�������ȣ�ClO2��Ϊһ�ֻ���ɫ���壬�ǹ����Ϲ��ϵĸ�Ч�����ס����١���ȫ��ɱ����������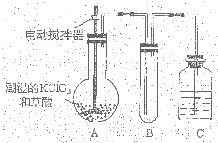 �������ȣ�ClO2����һ�ֻ���ɫ�д̼�����ζ�����壬���۵�Ϊ-59�棬�е�Ϊ11.0�棬������ˮ��ClO2���Կ����������ᣨHClO2�������ᣨHClO3���Ļ����������ҵ�����Գ�ʪ��KClO3�Ͳ��ᣨH2C2O4����60��ʱ��Ӧ�Ƶã�ijѧ��������ͼ��ʾװ��ģ�ҵ��ȡ���ռ�ClO2�����г�������ʡ�ԣ����ش����⣺
�������ȣ�ClO2����һ�ֻ���ɫ�д̼�����ζ�����壬���۵�Ϊ-59�棬�е�Ϊ11.0�棬������ˮ��ClO2���Կ����������ᣨHClO2�������ᣨHClO3���Ļ����������ҵ�����Գ�ʪ��KClO3�Ͳ��ᣨH2C2O4����60��ʱ��Ӧ�Ƶã�ijѧ��������ͼ��ʾװ��ģ�ҵ��ȡ���ռ�ClO2�����г�������ʡ�ԣ����ش����⣺