题目内容
某地甲、乙两工厂排放的污水中各含有下列8种离子中的4种(两厂废水所含离子不同):Ag+、Ba2+、Fe2+、Na+、Cl-、SO42-、NO3-、OH-。若两厂单独排放污水都会造成较严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便能变得无色澄清的只含硝酸钠的溶液而排放,污染程度大大降低。根据所给信息有以下几种说法,你认为正确的是( )
A.Na+和NO3-来自同一工厂 B.Cl-和Fe2+一定来自同一工厂
C.SO42-和Cl-来自同一工厂 D.Ag+和Na+可能来自同一工厂
练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
16.下列解释实验事实的方程式正确的是( )
| A. | CuSO4溶液中加入过量氨水得到深蓝色溶液:Cu2++2OH-═Cu(OH)2↓ | |
| B. | 碳酸钠溶液中滴入酚酞试液,溶液变红:CO32-+2H2O?H2CO3+2OH- | |
| C. | FeCl2溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ | |
| D. | 90℃时,测得纯水pH=6.7,pH<7的原因是:H2O(l)?H+(aq)+OH-(aq)△H<0 |
14.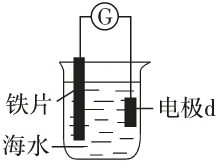 研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )
研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )
 研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )
研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )| A. | d为石墨,铁片腐蚀加快 | |
| B. | d为石墨,石墨上电极反应为:O2+2H2O+4e-=4OH- | |
| C. | d为锌块,铁片不易被腐蚀 | |
| D. | d为锌块,铁片上电极反应为:2H++2e-→H2↑ |
14.CO2溶于水生成碳酸.已知下列数据:
现有常温下1mol•L-1的(NH4)2CO3溶液,已知NH4+的水解平衡常数Kh=$\frac{{K}_{w}}{{K}_{b}}$,CO32-第一步水解的平衡
常数Kh=$\frac{{K}_{w}}{{K}_{{a}_{2}}}$.下列说法正确的是.
| 若电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数(25℃) | ${K}_{{a}_{1}}$=4.30×107 ${K}_{{a}_{2}}$=5.61×10-11 | Kh=1.77×10-5 |
常数Kh=$\frac{{K}_{w}}{{K}_{{a}_{2}}}$.下列说法正确的是.
| A. | 由数据可判断该溶液呈酸性 | |
| B. | c(NH4+)>c(HCO32-)>c(CO32-)>c(NH3•H2O) | |
| C. | c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| D. | c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
13.三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调节NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解.电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.以下说法正确的是( )
| A. | 可用铁作阳极材料 | |
| B. | 电解过程中阳极附近溶液的pH升高 | |
| C. | 阳极反应方程式为:2Cl--2e-═Cl2↑ | |
| D. | 1 mol二价镍全部转化为三价镍时,外电路中通过 了2 mol 电子 |


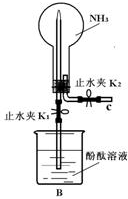 (1)甲同学用如图B装置做NH3喷泉实验,关闭K2,打开K1,用手捂热圆底烧瓶,一段时间后看到烧瓶内有红色喷泉现象.
(1)甲同学用如图B装置做NH3喷泉实验,关闭K2,打开K1,用手捂热圆底烧瓶,一段时间后看到烧瓶内有红色喷泉现象. 向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象_______________________。
向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象_______________________。