题目内容
14.下列关于胶体和溶液的叙述正确的是( )| A. | 胶体带电荷,而溶液呈电中性 | |
| B. | 胶体中加入电解质可以产生沉淀,而溶液不能 | |
| C. | 胶体是一种不稳定分散系,而溶液是一种最稳定分散系 | |
| D. | 胶体具有丁达尔效应,而溶液不具有 |
分析 A、从胶体分散系呈电中性分析;
B、根据胶体聚沉的条件和复分解的条件分析;
C、胶体较稳定,溶液稳定;
D、丁达尔效应是胶体特有的性质.
解答 解:A、溶液呈电中性,胶体分散系不带电,是胶体粒子吸附带电离子,故A错误;
B、胶体加入电解质溶液会发生聚沉可产生沉淀,复分解发生的条件之一是生成沉淀,所以溶液可以生成沉淀,溶液氢氧化钡与硫酸钠反应生成硫酸钡沉淀,故B错误;
C、胶体较稳定,是一种介稳性的分散系,溶液是一种非常稳定的分散系,故C错误;
D、丁达尔效应是胶体特有的性质,溶液没有丁达尔效应,故D正确,
故选D.
点评 本题考查了胶体和溶液中分散质的组成和性质,题目较简单,注意分析胶粒带电的原因和溶液中溶质的类别.

练习册系列答案
相关题目
10.下列实验的设计可行的是( )
| A. | 用澄清石灰水可区别Na2CO3和NaHCO3粉末 | |
| B. | 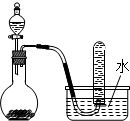 用如图装置进行浓硝酸与铜的反应制取并收集NO2 用如图装置进行浓硝酸与铜的反应制取并收集NO2 | |
| C. | 检验未知溶液是否含SO42ˉ可先加氯化钡,再加稀盐酸 | |
| D. | 除去粗盐中的Ca2+、Mg2+、SO42-,可依次加入H2O、NaOH、BaCl2、Na2CO3,过滤再加入HCl |
11.一种元素最高价态的氧化物的水化物的化学式为H3XO4,则X的氢化物的化学式是( )
| A. | HX | B. | H2X | C. | XH3 | D. | XH4 |
2.海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案:
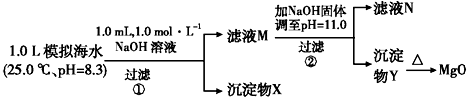
注:溶液中某种离子的浓度小于1.0×10-5 mol•L-1,可认为该离子不存在;
实验过程中,假设溶液体积不变.
KspCaCO3=4.96×10-9 KspMgCO3=6.82×10-6 KspCa(OH)2=4.68×10-6
KspMg(OH)2=5.61×10-12
下列说法不正确的是( )

| 模拟海水中的离 子浓度/mol•L-1 | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
实验过程中,假设溶液体积不变.
KspCaCO3=4.96×10-9 KspMgCO3=6.82×10-6 KspCa(OH)2=4.68×10-6
KspMg(OH)2=5.61×10-12
下列说法不正确的是( )
| A. | 沉淀物X为CaCO3、MgCO3 | |
| B. | 滤液M中存在Mg2+,Ca2+ | |
| C. | 滤液N中存在Ca2+,没有Mg2+ | |
| D. | 步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为仍Mg(OH)2,没有Ca(OH)2 |
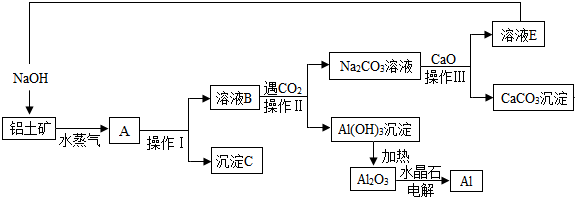
 (X)为卤素原子.
(X)为卤素原子.
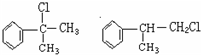 ;
; ;
;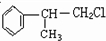 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$ +NaCl;
+NaCl; 或
或 .
.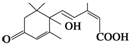 官能团的名称:碳碳双键、羰基、羟基、羧基.
官能团的名称:碳碳双键、羰基、羟基、羧基.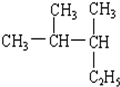 2,3-二甲基戊烷
2,3-二甲基戊烷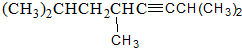 2,5,7-三甲基-3-辛炔
2,5,7-三甲基-3-辛炔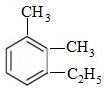
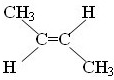 .
. 如图所示装置,c、d两极是石墨电极,回答下列问题:
如图所示装置,c、d两极是石墨电极,回答下列问题: