题目内容
(12分)化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,图中所列装置是用燃烧法确定有机物分子式常用的装置。完成下列问题:
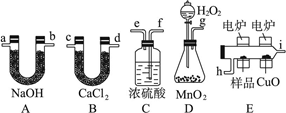
(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是________________。
(2)C装置中浓硫酸的作用是____________。(3)D装置中MnO2的作用是__________________。
(4)燃烧管中CuO的作用是__________________。
(5)若准确称取0.9 g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加1.32 g,B管质量增加0.54 g,则该有机物的实验式为__________________________。
(6)若该有机物溶于水,其分子式中氢原子为4,则其结构简式为______________。

(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是________________。
(2)C装置中浓硫酸的作用是____________。(3)D装置中MnO2的作用是__________________。
(4)燃烧管中CuO的作用是__________________。
(5)若准确称取0.9 g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加1.32 g,B管质量增加0.54 g,则该有机物的实验式为__________________________。
(6)若该有机物溶于水,其分子式中氢原子为4,则其结构简式为______________。
(1)g、f、e、h、i、c(或d)、d(或c)、a(或b)、b(或a)(也可考虑在末端再加ab,吸收空气中的水与二氧化碳)
(2)吸收水分,得干燥纯净的氧气 (3)催化剂,加快产生氧气的速率
(4)使有机物更充分地被氧化,生成二氧化碳和水 (5)CH2O (6) CH3COOH
(2)吸收水分,得干燥纯净的氧气 (3)催化剂,加快产生氧气的速率
(4)使有机物更充分地被氧化,生成二氧化碳和水 (5)CH2O (6) CH3COOH
试题分析:(1)首先对产生的氧气通过浓硫酸进行干燥,再将样品氧化,利用B、A吸收样品产生的水和二氧化碳。故各导管的连接顺序g、f、e、h、i、c(或d)、d(或c)、a(或b)、b(或a)。
(2)C装置中浓硫酸的作用是干燥氧气。
(3)D装置中MnO2的作用是做过氧化氢分解的催化剂,加快产生氧气的速率。
(4)防止一氧化碳的生成,再氧不充足时会生成一氧化碳,而氧化铜和一氧化碳反应生成二氧化碳,所以燃烧管中CuO的作用是使有机物更充分地被氧化,生成二氧化碳和水。
(5)A管质量增加1.32 g,为二氧化碳的质量,
m(C)=1.32g¸44g/mol´12g/mol=0.36g
B管质量增加0.54 g,为水的质量。
m(H)=0.54g¸18g/mol´2´1g/mol=0.06g
m(O)=0.9-0.36-0.06=0.48g
C、H、O原子个数比为:1:2:1,即实验式:CH2O
(6)该有机物溶于水,其分子式中氢原子为4,分子式为C2H4O2,为乙酸CH3COOH。
点评:本题考查了有机分子式的确定实验原理和相关计算。综合性较强。要求学生对有机分子式的确定方法比较熟悉。

练习册系列答案
相关题目
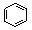 、
、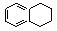 和
和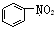 均属于芳香烃
均属于芳香烃