题目内容
某学生用滴定的方法测定含有少量NaCl的小苏打固体中NaHCO3的质量分数,所用标准盐酸的浓度为0.1000mol/L.关于该实验的叙述正确的是( )A.用烧杯准确配制100mL待测小苏打的溶液
B.用酚酞为指示剂
C.当滴至待测液变色并能将该颜色保持半分钟即为滴定终点
D.盛盐酸的滴定管未润洗会造成实验结果偏低
【答案】分析:A、根据烧杯只能粗略配制溶液;
B、根据NaHCO3完全反应应选择甲基橙作指示剂;
C、根据滴定终点时溶液颜色由黄色突变为橙色,且保持半分钟不变色;
D、根据c(待测)=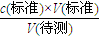 来分析.
来分析.
解答:解:A、烧杯只能粗略配制溶液,不能杯准确配制100mL待测小苏打的溶液,故A错误;
B、NaHCO3要完全反应应选择甲基橙作指示剂,故B错误;
C、滴定终点时溶液颜色由黄色突变为橙色,且保持半分钟不变色,故C正确;
D、盛盐酸的滴定管未润洗,标准液的浓度降低,造成V(标)偏大,根据c(待测)=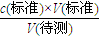 ,可知c(待测)偏大,故D错误;
,可知c(待测)偏大,故D错误;
故选C.
点评:本题考查中和滴定的操作以及注意事项,在误差分析时,无论哪一种类型的误差,都可以归结为对标准溶液体积的影响,其标准溶液的体积偏小,那么测得的物质的量的浓度也偏小;其标准溶液的体积偏大,那么测得的物质的量的浓度也偏大.
B、根据NaHCO3完全反应应选择甲基橙作指示剂;
C、根据滴定终点时溶液颜色由黄色突变为橙色,且保持半分钟不变色;
D、根据c(待测)=
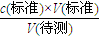 来分析.
来分析.解答:解:A、烧杯只能粗略配制溶液,不能杯准确配制100mL待测小苏打的溶液,故A错误;
B、NaHCO3要完全反应应选择甲基橙作指示剂,故B错误;
C、滴定终点时溶液颜色由黄色突变为橙色,且保持半分钟不变色,故C正确;
D、盛盐酸的滴定管未润洗,标准液的浓度降低,造成V(标)偏大,根据c(待测)=
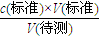 ,可知c(待测)偏大,故D错误;
,可知c(待测)偏大,故D错误;故选C.
点评:本题考查中和滴定的操作以及注意事项,在误差分析时,无论哪一种类型的误差,都可以归结为对标准溶液体积的影响,其标准溶液的体积偏小,那么测得的物质的量的浓度也偏小;其标准溶液的体积偏大,那么测得的物质的量的浓度也偏大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目