��Ŀ����
��һ�ݻ��̶����ܱ�������ͨ��A��B�������壬��һ��������ʹ֮��Ӧ��2A(��)��B(��) 2C(��)������ӦΪ���ȷ�Ӧ�����ﵽƽ��ı�����һ������(x)��������y�����ܷ���ͼ�����߱仯����
2C(��)������ӦΪ���ȷ�Ӧ�����ﵽƽ��ı�����һ������(x)��������y�����ܷ���ͼ�����߱仯����
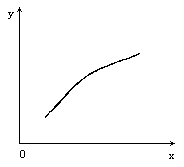
[����]
A����x��ʾѹǿʱ��y��ʾ��������ƽ��ʽ��
B����x��ʾ����A�����ʵ���ʱ��y��ʾC��Ũ��
C����x��ʾ����A�����ʵ���ʱ��y��ʾB��ת����
D����x��ʾ�¶�ʱ��y��ʾC�����ʵ���
������
|
���⣺Aѡ��ѹǿԽ��ƽ�������������С�ķ�������Ӧ�����ƶ������������ʵ�����С���������������䣬��������ƽ��ʽ������B��Cѡ�����A�����ʵ���ʱ��ƽ��������Ӧ�����ƶ���C���࣬B��ת��������������ѡ�����ͼ�⣮��Dѡ���¶�����ʱ��ƽ�����淴Ӧ�����ƶ���C���٣�����ͼ�⣮ |

 ���ʿ��ÿ��ֳɳ�ϵ�д�
���ʿ��ÿ��ֳɳ�ϵ�д��״���������10��һ25���ļ״�����������ԭ�ϡ����Ӽ��ϳɵ����ͳ���ȼ�ϣ��ɴﵽ�������͵����ܺ�ָ�ꡣ�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��ҵ�Ϻϳɼ״�һ��������з�Ӧ��CO��g��+2 H2��g�� CH3 OH��g�� ��H=a
kJ/mol��
CH3 OH��g�� ��H=a
kJ/mol��
�±��Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
|
�¶�/0C |
250 |
310 |
350 |
|
K |
2.041 |
0.250 |
0.012 |
��1���ɱ��������жϡ�H a 0���>������=����<������
��2��ij�¶��£���2 mol CO��6 mol H2����2 L���ܱ������У���ַ�Ӧ�ﵽƽ����c(CO)=0.5 mol��L��1�����ʱ���¶�Ϊ 0C��
��3�����ݻ��̶����ܱ������з���������Ӧ�������ʵ�Ũ�����±���
|
Ũ��mol/L ʱ��/min |
c(CO) |
c(H2) |
c(CH3OH)
|
|
0 |
0.8 |
1.6 |
0 |
|
2 |
0.6 |
1.2 |
0.2 |
|
4 |
0.3 |
0.6 |
0.5 |
|
6 |
0.3 |
0.6 |
0.5 |
�ٷ�Ӧ��2 min��4 min֮�䣬H2�ķ�Ӧ����Ϊ ��
�ڷ�Ӧ�ﵽƽ��ʱCO��ת����Ϊ ��
�۷�Ӧ�ڵ�2 minʱ�ı��˷�Ӧ�������ı������������ ������ţ���
A��ʹ�ô��� B�������¶� C������H2��Ũ��
��4�����ݻ���ͬ���¶ȷֱ�ΪT1��T2�������ܱ������о�����1 molCO��2 mol H2��������ӦCO��g��+2 H2��g��  CH3 OH��g����H=a kJ/mol�����º����·�Ӧ��ͬʱ��ֱ�����ϵ��CO�İٷֺ����ֱ�Ϊw1��w2����֪T1<T2����
CH3 OH��g����H=a kJ/mol�����º����·�Ӧ��ͬʱ��ֱ�����ϵ��CO�İٷֺ����ֱ�Ϊw1��w2����֪T1<T2����
w1 w2������ţ���
A������ B��С�� C������ D�����϶��п���
�״��ڻ�ѧ��Դ����Ҳ������ҪӦ�á�д���Լ״�Ϊȼ�ϣ�����������ҺΪ�������Һ��ԭ����и����ĵ缫��Ӧʽ�� ��
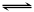 2Z(g)���ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��
2Z(g)���ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��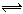 2Z(g)���ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��
2Z(g)���ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��