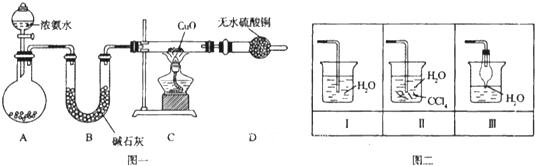
题目内容
(1)氨气极易溶于水,氨气与水反应的化学方程式为(2)在6份0.01mol/L的氨水中分别加入下列物质:
A.浓氨水B.纯水C.少量K2CO3 D.少量浓硫酸 E.少量NaOH固体 F.少量Al2(SO4)3固体.
①能使c(OH-)减少、c(NH4+)增大的是
②能使c(OH-)增大、c(NH4+)减少的是
③能使c(OH-)和c(NH4+)都增大的是
④能使c(OH-)和c(NH4+)都减少的是
分析:(1)氨气与水反应生成一水合氨,一水合氨为弱电解质,可电离出OH-,溶液呈碱性;
(2)氨水中存在NH3?H2O?NH4++OH-,结合浓度对电离平衡移动的影响解答.
(2)氨水中存在NH3?H2O?NH4++OH-,结合浓度对电离平衡移动的影响解答.
解答:解:(1)氨气与水反应生成一水合氨,方程式为NH3+H2O?NH3?H2O,一水合氨为弱电解质,可电离出OH-,溶液呈碱性,电离方程式为NH3?H2O?NH4++OH-,
故答案为:NH3+H2O?NH3?H2O;NH3?H2O?NH4++OH-;
(2)氨水中存在NH3?H2O?NH4++OH-,
①加入少量硫酸或硫酸铝,可生成水或氢氧化铝沉淀,使平衡向正向移动,则c(OH-)减少、c(NH4+)增大,故答案为:DF;
②能使c(OH-)增大、c(NH4+)减少,应加入碱或水解呈碱性的物质,则NaOH溶液以及少量K2CO3符合,故答案为:CE;
③加入浓氨水,可使c(OH-)和c(NH4+)都增大,故答案为:A;
④加水稀释时,可使c(OH-)和c(NH4+)都减少,故答案为:B.
故答案为:NH3+H2O?NH3?H2O;NH3?H2O?NH4++OH-;
(2)氨水中存在NH3?H2O?NH4++OH-,
①加入少量硫酸或硫酸铝,可生成水或氢氧化铝沉淀,使平衡向正向移动,则c(OH-)减少、c(NH4+)增大,故答案为:DF;
②能使c(OH-)增大、c(NH4+)减少,应加入碱或水解呈碱性的物质,则NaOH溶液以及少量K2CO3符合,故答案为:CE;
③加入浓氨水,可使c(OH-)和c(NH4+)都增大,故答案为:A;
④加水稀释时,可使c(OH-)和c(NH4+)都减少,故答案为:B.
点评:本题考查较为综合,涉及氨气的性质以及弱电解质的电离,为高频考点,侧重于学生的分析能力的考查,注意把握影响弱电解质的因素以及弱电解质的电离特点,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
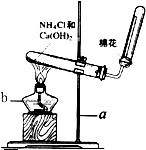 实验室常用下图装置制取氨气:请回答下列问题:
实验室常用下图装置制取氨气:请回答下列问题: