题目内容
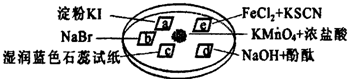
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加2滴浓盐酸后,立即用另一培养皿扣在上面.

已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是:
(1)a处变
(2)c处的现象为
(3)e处变
(4)近年来科学家提出,高铁酸钾(K2FeO4)也可用作水处理剂.可用FeCl3与KClO在强碱性条件下反应制取,其反应的离子方程式为(不需要配平)

已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是:
(1)a处变
蓝
蓝
色,b处变橙
橙
色;(2)c处的现象为
试纸先变红,后褪色
试纸先变红,后褪色
,请说明原因Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色
Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色
;(3)e处变
红
红
色,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
、Fe3++3SCN-=Fe(SCN)3
Fe3++3SCN-=Fe(SCN)3
;(4)近年来科学家提出,高铁酸钾(K2FeO4)也可用作水处理剂.可用FeCl3与KClO在强碱性条件下反应制取,其反应的离子方程式为(不需要配平)
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
.分析:Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变红棕色,可证明氧化性:Cl2>I2、Cl2>Br2,无法证明I2与Br2之间氧化性的强弱;C处先变红,说明氯气与水生成酸性物质,后褪色,则证明氯气与水生成具有漂白性物质;d处立即褪色,也可能是氯气与水生成酸性物质中和了NaOH;D处变红说明Cl2将Fe2+氧化为Fe3+,证明还原性:Fe2+>Cl-,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3;用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
解答:解:(1)Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变橙色,故答案为:蓝;橙;
(2)氯气与水反应Cl2+H2O=H++Cl-+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则C处先变红,后褪色,故答案为:先变红后褪色;Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色;
(3)Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3,
故答案为:红;2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3;
(4)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
(2)氯气与水反应Cl2+H2O=H++Cl-+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则C处先变红,后褪色,故答案为:先变红后褪色;Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色;
(3)Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3,
故答案为:红;2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3;
(4)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
点评:本题通过元素化合物知识,考查考生实验能力和对实验现象的分析、推断能力,题目难度中等,注意把握氯气以及其它物质的相关化学性质,把握离子方程式的书写方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面. 对实验现象的“解释或结论”正确的是( )
|
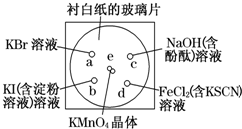 如图所示是验证氯气性质的微型实验,玻璃片上有a、b、c、d四滴溶液,向e处KMnO4晶体滴加一滴浓盐酸后,立即用一培养皿扣在玻璃片上.已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.下列有关说法不正确的是( )
如图所示是验证氯气性质的微型实验,玻璃片上有a、b、c、d四滴溶液,向e处KMnO4晶体滴加一滴浓盐酸后,立即用一培养皿扣在玻璃片上.已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.下列有关说法不正确的是( )| A、上述生成Cl2的反应中,HCl既表现出酸性又表现出还原性 | B、反应后a处呈橙色、b处呈蓝色、c处褪色、d处呈血红色 | C、a、b两处的颜色变化,证明单质氧化性:Cl2>Br2>I2 | D、d处的颜色变化,证明氧化性:Cl2>Fe3+;还原性:Cl-<Fe2+ |