题目内容
不同卤素原子间可以通过共用电子对,形成卤素互化物,其通式为:XX′n (n
= 1,3,5,7;且非金属性X′>X)。卤素互化物大多为强氧化剂。回答下列问题:
(1)卤素互化物中,沸点最低的应是 (写分子式,下同)。
(2)若n = 7,则最可能生成的卤素互化物应为 。
(3)现将23.3gBrCln溶于水,再通入过量SO2,生成HBr、HCl、H2SO4等三种酸,然后向该混合酸溶液中加入过量Ba(NO3)2溶液后,过滤,最后向滤液中加入过量的硝酸银溶液,结果可生成77.3g沉淀,求n的值(写出计算过程)。
(4)某卤素互化物与水的反应为 ClFn + H2O → HClO3 + Cl2 +O2 + HF,若ClFn与H2O的物质的量之比为3∶5,求n的值(写出计算过程)。
⑴ClF(2分) ⑵IF7(2分) ⑶n = 3(3分)
设BrCln的物质的量为x, 则
(80+35.5n)x = 23.3
(188+143.5n)x= 77.3 (2分)
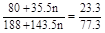
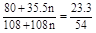 n = 3
(1分)
n = 3
(1分)
⑷(3分)由ClFn与H2O的物质的量之比为3∶5可得下列配平的方程式
3ClFn + 5H2O → (10-3n)HClO3 +(3n-7)∕2Cl2 +(9n-25)∕2O2 + 3nHF(1分)
所以有:
10-3n>0
(3n-7)∕2>0
(9n-25)∕2>0 (1分)n = 3 (1分)
其他解法合理即给分
【解析】略

 合酸溶液中加入过量Ba(NO3)2溶液后,过滤,最后向滤液中加入过量的硝酸银溶液,结果可生成77.3g沉淀,求n的值(写出计算过程)。
合酸溶液中加入过量Ba(NO3)2溶液后,过滤,最后向滤液中加入过量的硝酸银溶液,结果可生成77.3g沉淀,求n的值(写出计算过程)。