题目内容
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
|
⑨ |
⑦ |
⑧ |
|
根据元素在周期表中的位置可知,①~⑨分别是H、C、N、O、Na、Al、S、Cl、P。
Ⅰ、(1)元素⑦中质子数和中子数相等的原子符号是________________。
(2)④、⑤两种元素原子按1:1组成的常见化合物的化学式________________。
(3)③、⑧和⑨的最高价氧化物对应水化物的酸性由强到弱的顺序是________________。
(4)用电子式表示①和⑤形成化合物的过程_________________________。
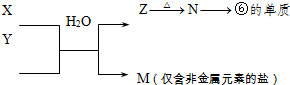
Ⅱ、由表中元素形成的物质A、B、C可发生以下反应(副产物已略去),试回答:

(1)若X是强氧化性单质,则A不可能是______________
a、S b、N2 c、Na d、Mg e、Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,检验此C溶液中金属离子的方法是____________________________________
__________________________;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式:___________________________________________。
(12分)Ⅰ、(1)3216S (2) Na2O2(3)HClO4﹥HNO3﹥H3PO4
(4)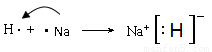
Ⅱ、(1)de (2)取少量试液于试管中,加入氢氧化钠溶液,产生白色沉淀随即变成灰绿色最后变成红褐色。(或先加入KSCN溶液无现象,通入氯气后呈血红色)(其他合理答案均可)。
2Fe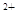 +H2O2+2H+=2Fe
+H2O2+2H+=2Fe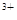 +2H2O((1)(2)1分其余每小题2分)
+2H2O((1)(2)1分其余每小题2分)
【解析】
试题分析:根据元素在周期表中的位置可知,①~⑨分别是H、C、N、O、Na、Al、S、Cl、P。据此可知:
Ⅰ、(1)元素⑦中质子数和中子数相等的原子符号是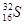 。
。
(2)④、⑤两种元素原子按1:1组成的常见化合物的化学式Na2O2。
(3)非金属性越强,最高价氧化物的水化物的酸性越强,则③、⑧和⑨的最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4﹥HNO3﹥H3PO4。
(4)①和⑤形成化合物NaH,含有离子键的离子化合物,所以用电子式表示①和⑤形成化合物的过程是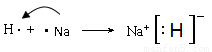 。
。
Ⅱ、(1)若X是强氧化性单质,则A可以是碳或S或氮气或进水钠等,但不可能是镁或铝,答案选de。
(2)若X是一种常见过渡金属单质,因此X是铁。向C的水溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,这说明C是氯化亚铁,则A是氯气,B是氯化铁。检验亚铁离子的方法是取少量试液于试管中,加入氢氧化钠溶液,产生白色沉淀随即变成灰绿色最后变成红褐色。(或先加入KSCN溶液无现象,通入氯气后呈血红色)(其他合理答案均可)。双氧水的还原产物是水,所以反应的离子方程式是2Fe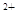 +H2O2+2H+=2Fe
+H2O2+2H+=2Fe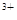 +2H2O。
+2H2O。
考点:考查元素周期表的结构以及元素周期律的应用和判断、元素及其化合物转化的有关判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案







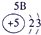
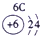
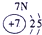
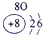
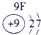
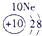
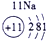





 表示的是
表示的是