��Ŀ����
������������ȷ����
- A.��a mol AlCl3����Һ�ͺ�1.5a mol NaOH����Һ���������κͷ��Σ����ɵ�Al(OH) 3���������
- B.��a mol Na2CO3����Һ�ͺ�1.5a mol HCl��ϡ����,�������κͷ���,���ɵ�CO2���
- C.��������NaHCO3��Na2CO3�ֱ����������ᷴӦ.��ͬ��ͬѹ��,���ɵ�CO2�����ͬ
- D.��ʢ��24mL NO2��O2�Ļ���������Ͳ������ˮ���У���ַ�Ӧ��ʣ��4 mL��ɫ���壬��ԭ���������O2�������8 mL �� 1.2mL
A
���������A�Al3+��OH����Ӧ���������������Al3++3OH��=Al(OH)3����Al3++4OH��=AlO2��+2H2O ,����n(Al3+):n(OH��)=2:3������Al3+���������������������ʵ���Ϊ0.5amol��A��ȷ��
B���a mol Na2CO3����Һ�еμӺ�1.5a mol HCl��ϡ���ᣬ�����ķ�Ӧ����ΪCO32��+H+=HCO3����HCO3��+H+=H2O+CO2��������CO2���ʵ���Ϊ0.5amol����1.5molHCl�������еμӺ�amolNa2CO3����Һ�������ķ�ӦΪCO32��+2H+=H2O+CO2��������CO2���ʵ���Ϊ0.75amol��B����
C���Na2CO3��CO2��NaHCO3��CO2��֪�����ʵ�����Na2CO3��NaHCO3����CO2���ʵ�����ȣ�C����
D���1����NO2��������ʣ������ΪNO����3NO2+H2O=2HNO3+NO��֪ʣ��NO212mL���ٸ���4NO2+O2+2H2O=4HNO3�ɵ�O2�����Ϊ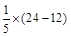 mL=2.4mL��
mL=2.4mL��
��2����O2��������ʣ������ΪO2���ɴ�4NO2+O2+2H2O=4HNO3��֪NO2���Ϊ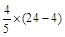 mL =16mL������O2Ϊ8mL��D����
mL =16mL������O2Ϊ8mL��D����
���㣺��ѧ����
���������⿼�黯ѧ��Ӧ���̺ͷ������۵�˼�롣
���������A�Al3+��OH����Ӧ���������������Al3++3OH��=Al(OH)3����Al3++4OH��=AlO2��+2H2O ,����n(Al3+):n(OH��)=2:3������Al3+���������������������ʵ���Ϊ0.5amol��A��ȷ��
B���a mol Na2CO3����Һ�еμӺ�1.5a mol HCl��ϡ���ᣬ�����ķ�Ӧ����ΪCO32��+H+=HCO3����HCO3��+H+=H2O+CO2��������CO2���ʵ���Ϊ0.5amol����1.5molHCl�������еμӺ�amolNa2CO3����Һ�������ķ�ӦΪCO32��+2H+=H2O+CO2��������CO2���ʵ���Ϊ0.75amol��B����
C���Na2CO3��CO2��NaHCO3��CO2��֪�����ʵ�����Na2CO3��NaHCO3����CO2���ʵ�����ȣ�C����
D���1����NO2��������ʣ������ΪNO����3NO2+H2O=2HNO3+NO��֪ʣ��NO212mL���ٸ���4NO2+O2+2H2O=4HNO3�ɵ�O2�����Ϊ
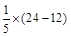 mL=2.4mL��
mL=2.4mL����2����O2��������ʣ������ΪO2���ɴ�4NO2+O2+2H2O=4HNO3��֪NO2���Ϊ
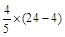 mL =16mL������O2Ϊ8mL��D����
mL =16mL������O2Ϊ8mL��D�������㣺��ѧ����
���������⿼�黯ѧ��Ӧ���̺ͷ������۵�˼�롣

��ϰ��ϵ�д�
�����Ŀ

 �����
����� 