题目内容
0.75 mol·L-1的NaOH溶液200 mL和0.5 mol·L-1的H3PO4溶液200 mL混合,生成盐的物质的量浓度接近( )A.NaH2PO4和Na2HPO4溶液的浓度均为0.2 mol·L-1
B.Na2HPO4和NaH2PO4溶液的浓度均为0.125 mol·L-1
C.0.15 mol·L-1的Na2HPO4和0.10 mol·L-1的NaH2PO4
D.0.1 mol·L-1的Na2HPO4和0.1 mol·L-1的Na3PO4
B
解析:n(NaOH)=0.75 mol·L-1×0.2 L=0.15 mol
n(H3PO4)=0.5 mol·L-1×0.2 L=0.1 mol,则n(NaOH)∶n(H3PO4)=3∶2,
可写出方程式:2H3PO4+3NaOH====Na2HPO4+NaH2PO4+3H2O,
故n(Na2HPO4)=n(NaH2PO4)=![]() =0.05 mol,
=0.05 mol,
c(Na2HPO4)=c(NaH2PO4)=![]() =0.125 mol·L-1。
=0.125 mol·L-1。

练习册系列答案
相关题目
下列溶液经反应后,溶液内含有0.50mol NaHCO3和0.50mol Na2CO3的是( )
| A、0.50L 1.00 mol?L-1 NaHCO3加0.50L 0.50 mol?L-1 NaOH | B、0.50L 0.75 mol?L-1 Na2CO3加0.50L 0.50 mol?L-1 HCl | C、0.50L 1.00 mol?L-1 NaHCO3 加0.50L 0.25 mol?L-1 NaOH | D、1.00L 1.00 mol?L-1 Na2CO3 加1.00L 0.50 mol?L-1 HCl |
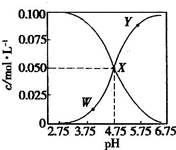 25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol?L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关离子浓度关系的叙述中正确的是( )
25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol?L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关离子浓度关系的叙述中正确的是( )