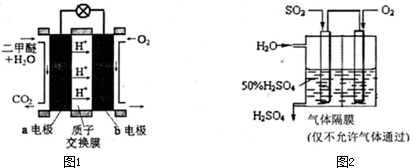
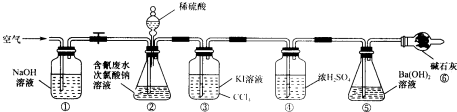
题目内容
利用图6-4所示装置,可进行若干实验。 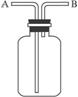
图6-4
(1)若用此干燥装置从A口进气收集气体X,则气体X应满足的条件是________________。
(2)若此装置充满水,用来测量气体Y的体积,气体Y应满足的条件是______________,此时气体从__________口进入集气瓶。
(3)若用此装置来除去气体中的某些杂质气体,则保留气体应满足的条件是______________,此时气体从________________进入集气瓶。
解析:(1)从A口进气收集气体的方法是向上排空气法,则气体X密度比空气大得多;(2)收集气体Y的方法是排水法,Y应难溶于水且与水不反应,收集时气体应从短进长出;(3)除去气体中的某些杂质气体,应长进短出。
答案:(1)密度比空气大很多的气体
(2)气体Y难溶于水且不与水反应 B
(3)不与洗气瓶中洗液反应且在洗液中不溶解 A口

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
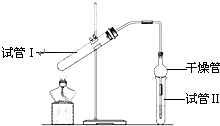 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图的装置制备乙酸乙酯.
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图的装置制备乙酸乙酯.(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验.实验开始先用酒精灯
微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中 试剂 |
有机层的 厚度/cm |
| A | 2mL乙醇、1mL乙酸、 1mL18mol?L-1 浓硫酸 |
饱和Na2CO3 溶液 |
3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、 3mL 2mol?L-1H2SO4 |
0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验
(3)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为