题目内容
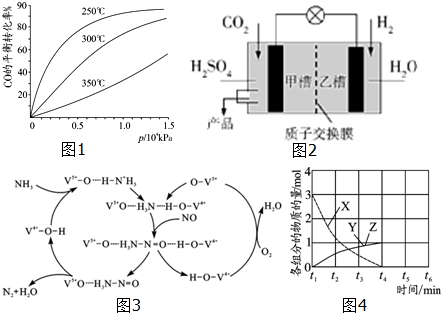
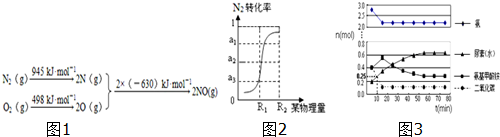
5.(1)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气.其中生成NO的能量变化示意图如图1:①该反应的热化学方程式为N2(g)+O2(g)=2NO(g)△H=+183kJ•mol-1.
②根据图2所示,只改变条件R,当N2的转化率从a3到a1时,平衡常数KA、C.
A.可能增大 B.一定不变 C.可能不变
D.可能减小 E.增大、减小、不变均有可能
(2)尿素(又称碳酰胺)是含氮量最高的氮肥,工业上利用CO2和NH3在一定条件下合成尿素的反应分为:
第一步:2NH3(g)+CO2(g)?H2NCOONH4(氨基甲酸铵) (l)
第二步:H2NCOONH4(l)?H2O(g)+H2NCONH2(l)
某实验小组模拟工业上合成尿素的条件,在一体积为500L的密闭容器中投入4mol氨和1mol二氧化碳,验测得反应中各组分的物质的量随时间的变化如图3所示:
①合成尿素总反应的快慢由第二步反应决定.
②反应进行到10min时测得 CO2的物质的量如3图所示,则用CO2表示的第一步反应的速率v(CO2)=1.5×10-4mol/(L•min).
③由氨基甲酸铵和CO2曲线变化可得出关于浓度变化和平衡状态的两条结论是:
a.氨基甲酸铵浓度先增大,15min后减小;
b.15min时第一步反应达到平衡状态,55min第二步反应达到平衡状态.
分析 (1)①根据能量变化图计算反应热,反应热=反应物的键能和-生成物的键能和,从而书写热化学方程式;
②平衡向正反应方向移动,则N2的转化率增大,可采用的方法为升高温度或者增加氧气的量;
(2)①已知总反应的快慢由慢的一步决定,结合图象变化趋势进行判断,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;
②分析图象计算10分钟时二氧化碳的消耗物质的量,结合化学反应速率概念进行计算;
③分析图象曲线的变化,氨基甲酸铵是随时间变化到15min物质的量增大,之后减小,15min时第一步反应达到平衡状态,55min氨基甲酸铵物质的量不再变化,第二步反应达到平衡状态.
解答 解:(1)①该反应中的反应热=反应物的键能和-生成物的键能和=(946+498)kJ/mol-2×630kJ/mol=+184kJ/mol,所以N2和O2反应生成NO的热化学反应方程式为N2(g)+O2(g)=2NO(g)△H=+183kJ•mol-1;
故答案为:N2(g)+O2(g)=2NO(g)△H=+183kJ•mol-1;
②只改变条件R,当N2的转化率从a3到a1时,平衡向正反应方向移动,则N2的转化率增大,可采用的方法为升高温度K增大或者增加氧气的量K不变,故选:A、C;
(2)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化,发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二部反应,从曲线斜率不难看出第二部反应速率慢,已知总反应的快慢由慢的一步决定,故合成尿素总反应的快慢由第二步决定,
故答案为:二;
②依据图象分析,二氧化碳再进行到10min时物质的量为0.25mol,所以此时的反应速率为=$\frac{\frac{1mol-0.25mol}{500L}}{10min}$=1.5×10-4mol/(L•min),
故答案为:1.5×10-4;
③分析图象曲线的变化,氨基甲酸铵物质的量随时间变化,到15min物质的量最大,之后减小,上图中氨气物质的量不变,15min时第一步反应达到平衡状态,55min氨基甲酸铵物质的量不再变化,第二步反应达到平衡状态;
故答案为:氨基甲酸铵浓度先增大,15min后减小;15min时第一步反应达到平衡状态,55min第二步反应达到平衡状态.
点评 本题考查了热化学方程式的计算分析,化学反应速率、平衡常数和化学平衡状态的分析判断,主要是图象变化的分析应用,掌握基础是解题关键,题目难度中等.


| A. | 有机物A不能使溴的四氯化碳溶液褪色 | |
| B. | 胡妥油可以发生加成反应和氧化反应 | |
| C. | 有机物A与胡妥油互为同系物 | |
| D. | 1 mol胡妥油完全燃烧消耗313.6 L的氧气 |
| A. | C3H8 | B. | C4H10 | C. | C6H14 | D. | C8H18 |
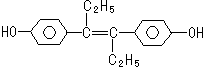
| A. | 己烯雌酚的分子式为C18H20O2 | |
| B. | 己烯雌酚可与NaOH和NaHCO3发生反应 | |
| C. | 1 mol该有机物可以与5 mol Br2发生反应 | |
| D. | 该有机物最多可能有18个碳原子共面 |
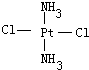 . 黄绿色固体:
. 黄绿色固体: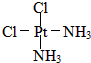 .
. ;该元素位于第三周期,第ⅢA族.
;该元素位于第三周期,第ⅢA族.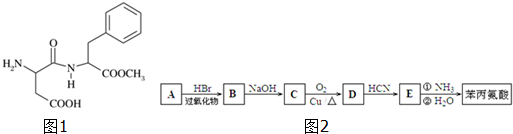
 )是合成APM的原料之一.苯丙氨酸的一种合成途径如图2所示:
)是合成APM的原料之一.苯丙氨酸的一种合成途径如图2所示: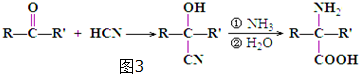
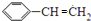 .
.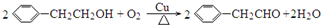 .
.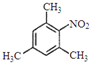 .
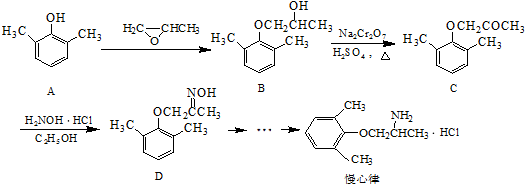
.
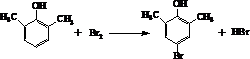 .
.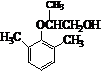 .
.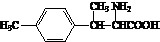 .
.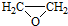 ).写出以邻甲基苯
).写出以邻甲基苯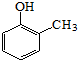 )和乙醇为原料制备
)和乙醇为原料制备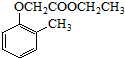 的合成路线流程图(无机试
的合成路线流程图(无机试