题目内容
9.下列做法不能使CaCO3+2HCl=CaCl2+CO2↑+H2O的反应速率增大的是( )| A. | 把2 mol/L盐酸换成2 mol/L H2SO4 | B. | 碾碎碳酸钙 | ||
| C. | 适当加热 | D. | 增大盐酸的浓度 |
分析 增大反应物浓度、升高温度、增大反应物接触面积等都能增大反应速率,据此分析解答.
解答 解:A.将盐酸换为等浓度的硫酸,氢离子浓度增大,但硫酸和碳酸钙反应生成微溶物硫酸钙,阻止进一步反应,所以反应速率降低,故A选;
B.碾碎碳酸钙,增大反应物接触面积,增大反应速率,故B不选;
C.适当升高温度,增大活化分子百分数,增大反应速率,故C不选;
D.增大盐酸浓度,单位体积内活化分子含量增大,所以反应速率增大,故D不选;
故选A.
点评 本题考查化学反应速率影响因素,侧重考查学生分析判断能力,明确反应速率影响因素及其原理是解本题关键,易错选项是A,注意硫酸钙的微溶性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列有关胶体的说法不正确的是( )
| A. | 电泳现象可证明胶体带有电荷 | |
| B. | 分散质粒子直径介于10-9 m~10-7m之间的分散系称为胶体 | |
| C. | 向Fe(OH)3胶体中滴入少量稀H2SO4,有红褐色沉淀产生 | |
| D. | 放电影时,放映室射到银幕上的光柱的形成属于丁达尔效应 |
4.下列4种有机化合物中,能够发生酯化、加成和氧化3种反应是( )
| A. | CH2=CHCOOH | B. | CH2=CHCOOCH3 | C. | CH2=CHCH2OH | D. | CH3CH2CH2OH |
17.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0L1.0mol•L-1的NaClO水溶液中含有的氧原子数为NA | |
| B. | 总质量为ag的CO和N2的混合物中所含原子总数为$\frac{a{N}_{A}}{14}$ | |
| C. | 2.24L 的2H35Cl分子中的中子数是1.9NA | |
| D. | 某密闭容器中盛有0.1mol N2和0.3molH2,在一定条件下充分反应,形成N-H键的数目为0.6NA |
4.市场上出现了各种各样的营养食盐,如锌营养盐、钙营养盐、硒营养盐、低钠营养盐、加碘食盐等十多种营养及保健盐.下列说法不正确的是( )
| A. | 加碘食盐是在食盐中加入了碘的化合物 | |
| B. | 钙营养盐是在食盐中加入了氯化钙或碳酸钙等含钙的化合物 | |
| C. | 低钠盐中的钠离子比氯离子少,所以低钠盐是一种带负电的物质 | |
| D. | 各类营养盐的主要成分都是氯化钠 |
14.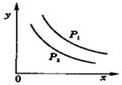 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )| A. | 上述正反应是放热反应 | B. | 上述正反应是吸热反应 | ||
| C. | 增大L的量,平衡正向移动 | D. | a<b |
19.下列物质中,不与溴水发生反应是( )
①乙苯 ②1,3-丁二烯 ③己烷 ④溴乙烷 ⑤乙酸 ⑥苯酚.
①乙苯 ②1,3-丁二烯 ③己烷 ④溴乙烷 ⑤乙酸 ⑥苯酚.
| A. | 只有① | B. | 只有①、③、④、⑤ | C. | 只有③、④、⑥ | D. | 只有①、③ |
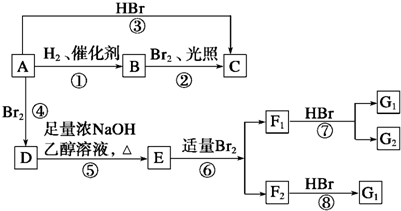
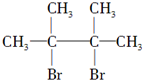 .
. ,其名称为2,3-二甲基-2-丁烯.
,其名称为2,3-二甲基-2-丁烯. .
.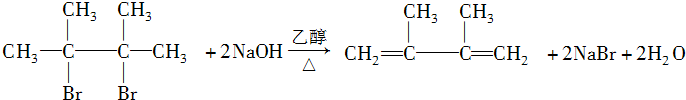 ;写出由E→F2的化学方程式:
;写出由E→F2的化学方程式: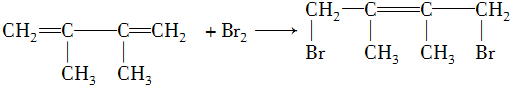 .
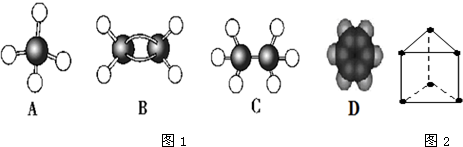
.
 .
.