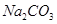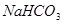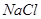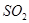题目内容
某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同
学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]
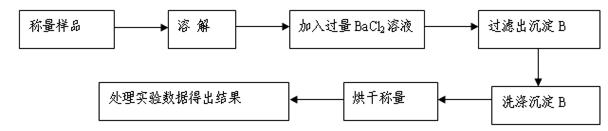
(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为 。
(2)洗涤沉淀B的操作是 。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________。
方案Ⅱ.乙组同学的主要实验流程图如下:
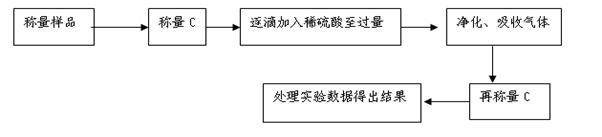
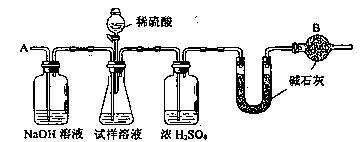
按如下图所示装置进行实验:
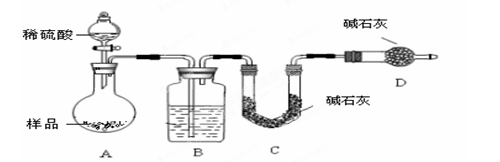
(4)该实验中装置B盛放的物质是_____________________,分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差
____________________。(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________________。
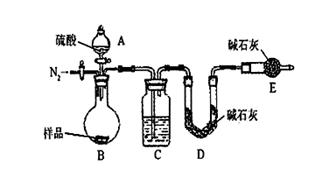
(6)有的同学认为为了减少实验误差,在反应前后都要通入N2(如右图),反应后通入N2的目的是____
__________________________________________________________________________________。
学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]

(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为 。
(2)洗涤沉淀B的操作是 。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________。
方案Ⅱ.乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:

(4)该实验中装置B盛放的物质是_____________________,分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差
____________________。(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________________。
(6)有的同学认为为了减少实验误差,在反应前后都要通入N2(如右图),反应后通入N2的目的是____
__________________________________________________________________________________。

(1)烧杯(2分)
(2)用玻璃棒引流,注入蒸馏水,直至刚好没过沉淀,待水从漏斗底部自然流完后,重复上述操作2-3次。(2分)
(3)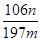 ×100%(2分) (4)浓硫酸 不能(各1分)
×100%(2分) (4)浓硫酸 不能(各1分)
(5)① 越小(2分) ②吸收空气中的水蒸气和二氧化碳,以确保前一个干燥管中质量增加量的准确性。(答案合理即可)(2分)
(6)将B、C装置中残留CO2全部驱入D装置的碱石灰中,减小实验误差。(2分)
(2)用玻璃棒引流,注入蒸馏水,直至刚好没过沉淀,待水从漏斗底部自然流完后,重复上述操作2-3次。(2分)
(3)
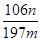 ×100%(2分) (4)浓硫酸 不能(各1分)
×100%(2分) (4)浓硫酸 不能(各1分)(5)① 越小(2分) ②吸收空气中的水蒸气和二氧化碳,以确保前一个干燥管中质量增加量的准确性。(答案合理即可)(2分)
(6)将B、C装置中残留CO2全部驱入D装置的碱石灰中,减小实验误差。(2分)
试题分析:(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为烧杯。
(2)过滤后沉淀的洗涤是在过滤器中完成的,所以洗涤沉淀B的操作是用玻璃棒引流,注入蒸馏水,直至刚好没过沉淀,待水从漏斗底部自然流完后,重复上述操作2-3次。
(3)能和氯化钡反应生成沉淀的是碳酸钠,即B是碳酸钡。所以若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钡的质量就是ng,物质的量=
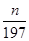 mol,因此根据CO32-守恒可知,碳酸钠的物质的量也是
mol,因此根据CO32-守恒可知,碳酸钠的物质的量也是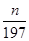 mol,质量=
mol,质量=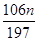 g,则碳酸钠的质量分数为
g,则碳酸钠的质量分数为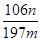 ×100%。
×100%。(4)由于碱石灰也能吸收水蒸气和氯化氢,而生成的CO2气体中含有水蒸气,所以B中盛放的应该是浓硫酸,用来干燥CO2。又因为盐酸易挥发,如果用盐酸代替稀硫酸,则生成的CO2气体中混有氯化氢气体,碱石灰吸收氯化氢,导致测量的CO2质量不准确,因此不能用盐酸代替稀硫酸。
(5)①由于在质量相等的条件下,碳酸氢钠与稀硫酸反应放出的CO2气体多,所以样品中碳酸钠的质量分数越大,生成的CO2越少,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差越小。
②由于空气中也含有水蒸气、CO2,所以D装置中碱石灰的作用是吸收空气中的水蒸气和二氧化碳,以确保前一个干燥管中质量增加量的准确性。
(6)由于装置中含有空气,所以实验前通入氮气的目的是排尽装置中的空气。而实验后装置还有未被吸收的CO2,所以实验后通入氮气的目的是将B、C装置中残留CO2全部驱入D装置的碱石灰中,减小实验误差。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目