题目内容
某二价金属碳酸盐和碳酸氢盐的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为6∶5,该混合物中碳酸盐和碳酸氢盐的物质的量之比为
| A.1∶1 | B.1∶2 | C.1∶3 | D.1∶4 |
B
设二价金属为M,正盐的物质的量为x mol,酸式盐的物质的量为y mol,则有:
MCO3+2HCl===MCl2+CO2↑+H2O
x 2x x
M(HCO3)2+2HCl===MCl2+2CO2↑+2H2O
y 2y 2y
由题意得: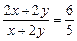 ,解得
,解得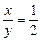 。
。
MCO3+2HCl===MCl2+CO2↑+H2O
x 2x x
M(HCO3)2+2HCl===MCl2+2CO2↑+2H2O
y 2y 2y
由题意得:
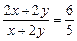 ,解得
,解得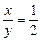 。
。
练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目