题目内容
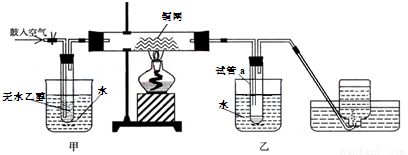
化学老师们在平时的教学过程中深入思考、积极探索将书本上的乙醇催化氧化的实验装置作如下改进,并用该装置进行演示实验:
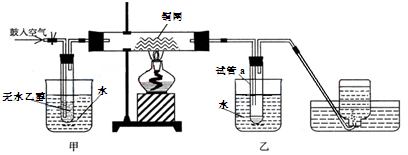
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:
在鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是
(2)甲和乙两个水浴的作用不相同.
甲的作用是:
(3)反应一段时间后,干燥试管a中能收集到不同的液态物质.它们是:
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
然后,再通过

(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:
2Cu+O2
2CuO、CH3CH2OH+CuO
CH3CHO+Cu+H2O
| ||
| △ |
2Cu+O2
2CuO、CH3CH2OH+CuO
CH3CHO+Cu+H2O
| ||
| △ |
在鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是
放热
放热
反应.(2)甲和乙两个水浴的作用不相同.
甲的作用是:
加热乙醇,便于乙醇的挥发
加热乙醇,便于乙醇的挥发
乙的作用是:冷却,便于乙醛的收集
冷却,便于乙醛的收集
(3)反应一段时间后,干燥试管a中能收集到不同的液态物质.它们是:
乙醛、乙醇、水
乙醛、乙醇、水
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
乙酸
乙酸
,要除去该物质,可以先在混合液中加入C
C
(填写字母)A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
然后,再通过
蒸馏
蒸馏
(填实验操作名称)即可除去.分析:(1)乙醇的催化氧化反应实质是:金属铜被氧气氧化为氧化铜,氧化铜将乙醇氧化为乙醛,金属铜起催化剂作用,该反应是放热反应;
(2)热水浴和冷水浴的作用是不同的,前者可以使温度升高,后者可以使的温度降低;
(3)根据反应过程中出现物质的沸点高低不同来确定出现的物质;
(4)能使紫色石蕊试纸变红的是酸,碳酸氢钠可以和乙酸反应,互溶液体的分离可以用蒸馏的方法.
(2)热水浴和冷水浴的作用是不同的,前者可以使温度升高,后者可以使的温度降低;
(3)根据反应过程中出现物质的沸点高低不同来确定出现的物质;
(4)能使紫色石蕊试纸变红的是酸,碳酸氢钠可以和乙酸反应,互溶液体的分离可以用蒸馏的方法.
解答:解:(1)乙醇的催化氧化反应过程:金属铜被氧气氧化为氧化铜,2Cu+O2
2CuO,氧化铜将乙醇氧化为乙醛,CH3CH2OH+CuO
CH3CHO+Cu+H2O,该反应是放热反应,
故答案为:2Cu+O2
2CuO、CH3CH2OH+CuO
CH3CHO+Cu+H2O;放热;
(2)甲和乙两个水浴作用不相同,甲是热水浴,作用是乙醇平稳气化成乙醇蒸气,起到加热的作用,乙是冷水浴,目的是将乙醛冷却下来,
故答案为:加热乙醇,便于乙醇的挥发;冷却,便于乙醛的收集;
(3)乙醇的催化氧化实验中的物质中:乙醛、乙醇和水的沸点高低不同,依次升高,在试管a中按照沸点从低到高可以收集到乙醛、乙醇、水,
故答案为:乙醛、乙醇、水;
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,四个选择答案中,只有碳酸氢钠可以和乙酸反应,生成乙酸钠、水和二氧化碳,实现两种互溶物质的分离用蒸馏法,故答案为:乙酸;C;蒸馏.
| ||
| △ |
故答案为:2Cu+O2
| ||
| △ |
(2)甲和乙两个水浴作用不相同,甲是热水浴,作用是乙醇平稳气化成乙醇蒸气,起到加热的作用,乙是冷水浴,目的是将乙醛冷却下来,
故答案为:加热乙醇,便于乙醇的挥发;冷却,便于乙醛的收集;
(3)乙醇的催化氧化实验中的物质中:乙醛、乙醇和水的沸点高低不同,依次升高,在试管a中按照沸点从低到高可以收集到乙醛、乙醇、水,
故答案为:乙醛、乙醇、水;
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,四个选择答案中,只有碳酸氢钠可以和乙酸反应,生成乙酸钠、水和二氧化碳,实现两种互溶物质的分离用蒸馏法,故答案为:乙酸;C;蒸馏.
点评:本题涉及化学实验基本、乙醇的催化氧化实验方面的知识,属于教材知识的考查,综合性较强,难度不是很大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
 Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
 CH3CHO+Cu+H2O
CH3CHO+Cu+H2O