题目内容
18.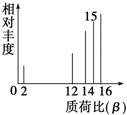 设H+的质荷比为β,其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )
设H+的质荷比为β,其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )| A. | 甲醇(CH3OH) | B. | 甲烷 | C. | 丙烷 | D. | 乙烯 |
分析 根据某有机物样品的质荷比的最大值为该物质的相对分子质量,然后根据相对分子质量来确定物质的分子式.
解答 解:由有机物样品的质荷比图,可知该物质的相对分子质量为16,甲醇、甲烷、丙烷、乙烯的相对分子质量分别为32、16、42、28,则该有机物甲烷,
故选B.
点评 本题主要考查了有机物样品的质荷比图的运用,根据原理即可解答,比较简单.

练习册系列答案
相关题目
8.下列有关糖类、油脂、蛋白质的说法正确的是( )
| A. | 蛋白质中只含C、H、O三种元素 | |
| B. | 许多油脂兼有烯烃和酯的性质,可以发生加成反应和水解反应 | |
| C. | 糖类的主要成分是高级脂肪酸甘油酯 | |
| D. | 所有糖、油脂、蛋白质都能发生水解反应 |
9.下列说法正确的是( )
| A. | 活化分子间所发生的碰撞为有效碰撞 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能增加单位体积内活化分子的百分数和活化分子总数使反应速率增大 | |
| D. | 缩小容器的体积而增大压强,可增加活化分子总数,从而使反应速率增大 |
6.下列变化过程中,同时有离子键、极性键、非极性键的断裂和形成的是( )
| A. | 2NH4HCO3=2NH3+CO2+2H2O | B. | 2NaOH+Cl2=NaCl+NaClO+H2O | ||
| C. | 2Na2O2+2CO2=2Na2CO3+O2 | D. | H2+Cl2=2HCl |
13.下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T形成的化合物具有两性 | D. | L2+与R2-的核外电子数相等 |
3.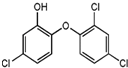 三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )
三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )
 三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )
三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )| A. | 该物质与浓溴水可发生取代反应 | |
| B. | 物质的分子式为C12H6Cl3O2 | |
| C. | 该物质中所有原子不一定在同一平面上 | |
| D. | 该物质苯环上的一溴取代物有6种 |
10.A、B、C、D、E是短周期主族元素,其原子序数依次增大.A元素的气态氢化物可以与A元素的最高价氧化物对应的水化物反应生成盐,B元素原子最外层电子数是次外层电子数的3倍,C、D、E处于同一周期,B和E处于同一族,B、E元素原子的核外电子数之和与C、D元素原子的核外电子数之和相等.下列说法不正确的是( )
| A. | B、C、D、E四种元素原子半径由大到小的顺序是:C>E>D>B | |
| B. | C和D两元素的最高价氧化物对应水化物的碱性:C>D | |
| C. | B和E两元素的气态氢化物热稳定性:B>E | |
| D. | A元素的气态氢化物与其最高价氧化物对应的水化物反应后产物中既含有离子键又含有共价键 |
7.下述情况下物质的量可能不相等的是( )
| A. | 密度相等,等体积的NO和 C2H6 (g) | B. | 常温常压下,等体积的NO和 C2H6 (g) | ||
| C. | 等温条件下,等体积的NO和 C2H6 (g) | D. | 常温常压下,等质量的NO和 C2H6 (g) |
20.下列物质中既有离子键又有共价键的可溶性化合物是( )
| A. | H2SO4 | B. | BaSO4 | C. | N2 | D. | NaOH |