题目内容
下列物质的除杂方法中,合理的是( )
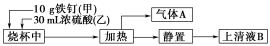
①C2H6中混有的C2H4,可以将混合气体先通过溴水,然后用碱石灰干燥
②K2CO3中混有的少量NaHCO3,可以用加热的方法除去
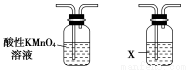
③乙烯中混有的SO2气体可以通过酸性高锰酸钾溶液除去
④金属铜中含有的少量银和锌可以通过电解精炼的方法除去
⑤H2S中混有的水蒸气用浓硫酸干燥即可
A.①④ B.②③ C.①⑤ D.④⑤
A
【解析】混有C2H4的C2H6,先通过溴水,C2H4与溴发生加成反应而被除去,后通过碱石灰干燥即可得到C2H6,①对;混有NaHCO3的K2CO3,加热时NaHCO3分解转化为Na2CO3,最终得到K2CO3和Na2CO3的混合物,②错;乙烯、SO2均能被酸性高锰酸钾溶液氧化,③错;电解精炼含Ag、Zn的粗铜时,Zn放电后进入溶液,Cu放电后进入溶液,Cu2+在阴极上反应得到纯铜,Ag形成阳极泥,④对;H2S具有还原性,能被浓硫酸氧化,⑤错。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在相同的温度下,体积均为0.25 L的两恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如表所示,下列叙述错误的是( )
2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如表所示,下列叙述错误的是( )
| 起始时各物质的物质 的量(mol) | 达到平衡时能量变化 | ||
容器编号 | N2 | H2 | NH3 | |
① | 1 | 3 | 0 | 放出23.15 kJ能量 |
② | 0.9 | 2.7 | 0.2 | 放出Q kJ能量 |
A.容器①、②中反应的化学平衡常数相等
B.平衡时,两容器中氨气的体积分数均为14.3%
C.反应②达到平衡时,放出的热量Q=23.15 kJ
D.若①的体积为0.5 L,则达到平衡时放出的热量小于23.15 kJ