题目内容
在一定条件下,化学反应N2+3H2?2NH3达到平衡状态的标志为( )
| A.容器内平均相对分子质量不随时间变化 |
| B.N2、H2、NH3的浓度之比为1:3:2 |
| C.N2减少的速率和NH3生成的速率之比为1:2 |
| D.气体体积为初始体积的一半 |
A、反应两边气体的化学计量数之和不相等,气体的质量不变,M=
,所以容器内平均相对分子质量不随时间变化,说明正逆反应速率相等,达到了平衡状态,故A正确;
B、浓度之比不能判断各组分的浓度是否变化,正逆反应速率是否相等,无法判断是否达到了平衡状态,故B错误;
C、氮气的减少和氨气的生成都是正反应速率,无法判断正逆反应速率相等,故C错误;
D、正反应是体积缩小的反应,气体体积为初始体积的一半,无法判断各组分的浓度是否不再变化,无法判断是否达到了平衡状态,故D错误;
故选:A.
| m |
| n |
B、浓度之比不能判断各组分的浓度是否变化,正逆反应速率是否相等,无法判断是否达到了平衡状态,故B错误;
C、氮气的减少和氨气的生成都是正反应速率,无法判断正逆反应速率相等,故C错误;
D、正反应是体积缩小的反应,气体体积为初始体积的一半,无法判断各组分的浓度是否不再变化,无法判断是否达到了平衡状态,故D错误;
故选:A.

练习册系列答案
相关题目
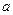 mol A和
mol A和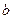 mol B在一个容积可变的容器中发生反应:A(g)+2B(g)
mol B在一个容积可变的容器中发生反应:A(g)+2B(g) 2C(g),一段时间后达到平衡,生成
2C(g),一段时间后达到平衡,生成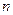 mol C。则下列说法中正确的是 ( )
mol C。则下列说法中正确的是 ( )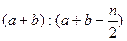
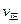 (A)=2
(A)=2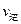 (B)时,可确定反应达平衡
(B)时,可确定反应达平衡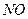 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的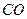 转变成
转变成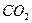 和
和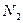 ,化学方程式如下:
,化学方程式如下:

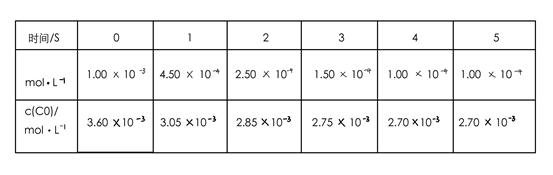
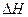 0(填写“>”、“<”、“=”。
0(填写“>”、“<”、“=”。