题目内容
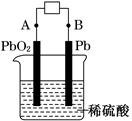
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4===2PbSO4+2H2O,下列结论正确的是 ( )
Pb+PbO2+2H2SO4===2PbSO4+2H2O,下列结论正确的是 ( )
| A.Pb为正极被氧化 | B.溶液的pH不断减小 |
| C.SO42-只向PbO2处移动 | D.电解质溶液pH不断增大 |
D
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据方程式可知,Pb失去电子,在负极被氧化。二氧化铅是正极,得到电子;反应中消耗硫酸,溶液中pH增大,阴离子向负极Pb移动,所以正确的答案选D。
点评:该题是中等难度的试题,试题基础性强,侧重对学生基础知识的巩固与训练,有助于调动学生的学习兴趣和学习积极性。该题的关键是明确原电池的工作原理,然后结合题意灵活运用即可。

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
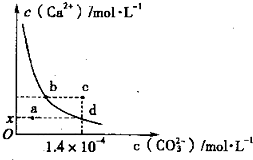
 2ZnO,下列判断正确的是( )
2ZnO,下列判断正确的是( )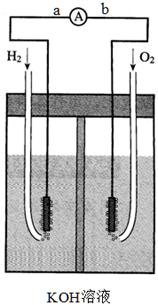
 2 CO32— + 6H2O,则下列说法错误的是
2 CO32— + 6H2O,则下列说法错误的是
 2PbSO4+2H2O
2PbSO4+2H2O