题目内容
20.完成下列填空.(1)写出下列物质的电子式:CO2
 Na2O2
Na2O2
(2)用电子式表示下列物质的形成过程:NH33H•+
 →
→ 、MgCl2
、MgCl2 .
.
分析 (1)二氧化碳中存在两个碳氧双键,C、O原子最外层都达到最外层8个电子;过氧化钠为含有非极性共价键的离子化合物,钠离子与过氧根中为离子键,过氧根中的两个氧原子间为共价键;
(2)氨气为共价化合物,根据共价化合物电子式的表示方法用电子式表示出氨气;镁原子最外层有两个电子易失去最外层的2个电子形成稳定的镁离子,卤原子最外层有7个电子,2个氯原子从镁原子分别得到1个电子形成稳定的氯离子,在镁离子与氯离子的静电作用下结合形成氯化镁;
解答 解:(1)二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为: ;Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为
;Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为 .故答案为:
.故答案为: ;
; ;
;
(2)NH3为共价化合物,用电子式表示氨气分子的形成过程为:3H•+ →
→ ;镁原子失去最外层的2个电子形成稳定的镁离子,2个氯原子从镁原子分别得到1个电子形成稳定的氯离子,在镁离子与氯离子的静电作用下结合形成氯化镁,用电子式表示下列物质的形成过程为:
;镁原子失去最外层的2个电子形成稳定的镁离子,2个氯原子从镁原子分别得到1个电子形成稳定的氯离子,在镁离子与氯离子的静电作用下结合形成氯化镁,用电子式表示下列物质的形成过程为: ;
;
点评 本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别,能够用电子式正确表示化合物的形成过程.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列对一些实验事实和理论解释正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | HCl气体溶于水,能导电 | HCl为离子化合物 |
| B | HBr的酸性强于HCl的酸性 | Br的非金属性比Cl强 |
| C | K3C60在熔融状态下能够导电 | K3C60中含有离子键 |
| D | HF的沸点高于HCl | HF分子间形成有氢键 |
| A. | A | B. | B | C. | C | D. | D |
11.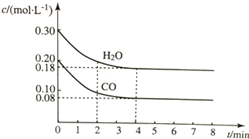 在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.
在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.
(1)则0~4min内反应速率v(CO)为0.03mol/(L•min);
(2)1000℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.
1000℃时物质浓度的变化
①c1数值>0.08mol/L(填“<”“>”或“=”);
②表中5~6min之间数值发生变化,可能的原因是a(填字母).
a.增加水蒸气
b.降低温度
c.使用催化剂
d.增加氢气浓度.
 在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.
在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.(1)则0~4min内反应速率v(CO)为0.03mol/(L•min);
(2)1000℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.
1000℃时物质浓度的变化
| t/min | c(CO)/(mol•L-1) | c(H2O)/(mol•L-1) | c(CO2)/(mol•L-1) | c(H2)/(mol•L-1) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 1 | 0.138 | 0.238 | 0.062 | 0.062 |
| 2 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | 0.084 |
| 6 | 0.096 | 0.266 | 0.104 | 0.104 |
②表中5~6min之间数值发生变化,可能的原因是a(填字母).
a.增加水蒸气
b.降低温度
c.使用催化剂
d.增加氢气浓度.
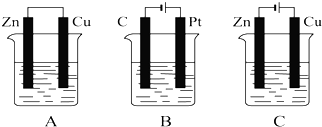
5.实验室制取氯气应该选用哪一套装置( )
| A. | 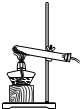 | B. | 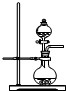 | C. | 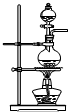 |
12.下列有关说法正确的是( )
| A. | NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 镀锡铁制品镀层破损后,铁制品比受损前更容易生锈,而镀锌铁制品则相反 | |
| C. | 将纯水加热至较高温度,K变大、pH变小、呈酸性 | |
| D. | 给0.1mol•L-1CH3COOH溶液中加热,则c(H+)与c(CH3COOH)的比值增大 |
9.下列物质中属于含有共价键的离子化合物的是( )
| A. | NaOH | B. | AlCl3 | C. | K2S | D. | Cl2 |
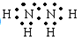 ,过氧化氢的结构式:
,过氧化氢的结构式: .
.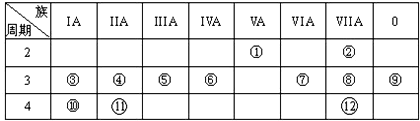
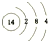 ,写出①的气态氢化物分子的电子式
,写出①的气态氢化物分子的电子式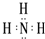 .
.