题目内容
16.常温下在稀溶液中能表示中和热的热化学方程式为( )| A. | H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l)△H1=aKJ•mol-1 | |
| B. | HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l)△H2=bKJ•mol-1 | |
| C. | HCl(aq)+NH3•H2O (aq)=NH4Cl(aq)+H2O(l)△H3=cKJ•mol-1 | |
| D. | H+(aq)+OH-(aq)+$\frac{1}{2}$Ba2+(aq)+$\frac{1}{2}$SO42-(aq)=$\frac{1}{2}$BaSO4(s)+H2O(l)△H4=dKJ•mol-1 |
分析 根据中和热的概念:稀的强酸和强碱反应生成1mol水所放出的热量为中和热.
解答 解:A.方程式中生成2mol水,中和热必须生成1mol水,故A错误;
B.生成1mol水,能表示中和热,故B正确;
C.NH3•H2O为弱碱,应用稀的强碱溶液,故C错误;
D.反应生成硫酸钡放热,△H4不是中和热,故D错误.
故选B.
点评 本题考查中和热以及热化学方程式的书写问题,本题难度中等,注意准确理解中和热的概念.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
12.已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是( )
| A. | A、B、D不可能在同周期 | B. | C和D的单质可能化合为离子化合物 | ||
| C. | A、D可能在同一主族 | D. | D一定在第二周期 |
4.某科研小组设计出利用工业废酸(稀H2SO4)来浸取某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如图所示.
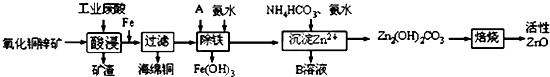
已知:各离子开始沉淀及完全沉淀时的pH如表所示.
请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是适当升高温度(或增大酸浓度、将氧化铜锌矿粉碎等).(任写一点即可)
(2)物质A最好使用下列物质中的B.
A.KMnO4B.H2O2C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2~6.2范围之间.
(4)物质B可直接用作氮肥,则B的化学式是(NH4)2SO4.
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能处理剂--K2FeO4,写出该反应的离子方程式2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.

已知:各离子开始沉淀及完全沉淀时的pH如表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是适当升高温度(或增大酸浓度、将氧化铜锌矿粉碎等).(任写一点即可)
(2)物质A最好使用下列物质中的B.
A.KMnO4B.H2O2C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2~6.2范围之间.
(4)物质B可直接用作氮肥,则B的化学式是(NH4)2SO4.
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能处理剂--K2FeO4,写出该反应的离子方程式2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.
1.已知下列反应的焓变:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3KJ•mol-1
(2)C(s)+O2(g)=CO2(g)△H2=-393.5KJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H3=-285.8KJ•mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变为( )
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3KJ•mol-1
(2)C(s)+O2(g)=CO2(g)△H2=-393.5KJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H3=-285.8KJ•mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变为( )
| A. | -870.3KJ•mol-1 | B. | -571.6KJ•mol-1 | C. | +787.0KJ•mol-1 | D. | -488.3KJ•mol-1 |
8.下列物质中,既有离子键又有共价键的是( )
| A. | CaCl2 | B. | KOH | C. | H2O | D. | HCl |
5.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断不正确的是( )
| 实验编号 | 起始浓度/(mol•L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A. | 实验①反应后的溶液中:c(HA)=c(OH-)-c(H+) | |
| B. | 实验①反应后的溶液中:c(OH-)=c(K+)+c(H+)-c(A-) | |
| C. | 实验②反应后的溶液中:c(A-)+c(HA)>0.2mol•L-1 | |
| D. | 实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+) |
6.下列说法中正确的是( )
| A. | 用完的电池可以随意地丢弃 | |
| B. | 增加炼铁高炉的高度可以降低尾气中CO的含量 | |
| C. | 实验室用一定质量的锌和过量的稀硫酸反应制取氢气时,加入少量硫酸铜可以加快反应速率且生成氢气的量不变 | |
| D. | 把煤粉碎后再燃烧可以提高煤的燃烧效率 |
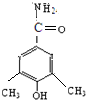
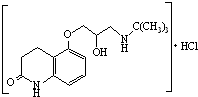 )可用于治疗心绞痛和青光眼.
)可用于治疗心绞痛和青光眼.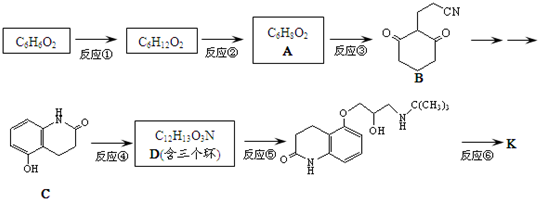
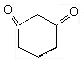 D
D
 、
、
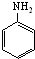 )与HNO2和H3PO2反应可得苯.请设计从C合成
)与HNO2和H3PO2反应可得苯.请设计从C合成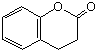 的路线.(合成路线常用的表示方法为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)
的路线.(合成路线常用的表示方法为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)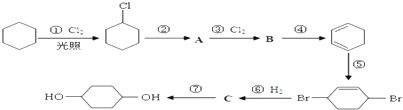
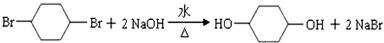 ;
;