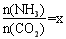题目内容
一定条件下,在密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g).当N2、H2、NH3的浓度不再改变时,下列说法正确的是( )
| A、N2、H2完全转化为NH3 | B、N2、H2、NH3的浓度一定相等 | C、反应已达到化学平衡状态 | D、正、逆反应速率相等且等于零 |
分析:当N2、H2、NH3的浓度不再改变时,即为化学平衡状态,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:解:A、任何可逆反应都不可能完全转化,所以N2、H2不可能完全转化为NH3,故A错误;
B、当体系达平衡状态时,N2、H2、NH3的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故B错误;
C、反应已达到化学平衡状态,说明N2、H2、NH3的浓度不再改变,故C正确;
D、化学平衡是动态平衡,正、逆反应速率相等且大于零,故D错误;
故选C.
B、当体系达平衡状态时,N2、H2、NH3的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故B错误;
C、反应已达到化学平衡状态,说明N2、H2、NH3的浓度不再改变,故C正确;
D、化学平衡是动态平衡,正、逆反应速率相等且大于零,故D错误;
故选C.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
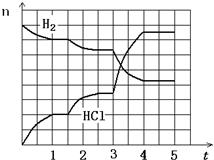 (2013?河东区一模)工业上高纯硅可以通过下列反应制取:
(2013?河东区一模)工业上高纯硅可以通过下列反应制取: