��Ŀ����
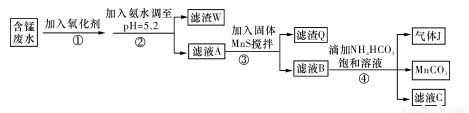
���ú��̷�ˮ����Ҫ��Mn2+��SO42-��H+��Fe2+��Al3+��Cu2+�����Ʊ������ܴ��Բ���̼���̣�MnCO3��������һ�ֹ�ҵ�������£�
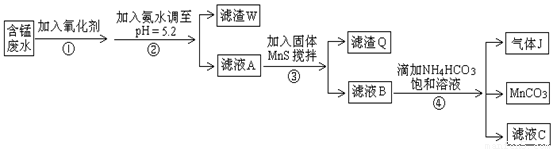
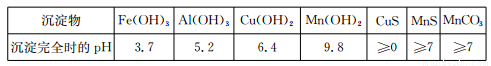
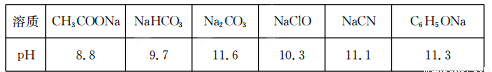
��֪ijЩ������ȫ������pHֵ���±���
|
������ |
Fe(OH)3 |
Al(OH)3 |
Cu(OH)2 |
Mn(OH)2 |
CuS |
MnS |
MnCO3 |
|
������ȫʱ��PH |
3.7 |
5.2 |
6.4 |
9.8 |
��0 |
��7 |
��7 |
�ش��������⣺
��1�����������ʾ��ܰ�Fe2+����ΪFe3+������̢��п�ѡ�������������� ��
a��Cl2 b��MnO2 c��ŨHNO3 d��H2O2
��2�����̢��У����������ijɷ��� ��
��3�����̢��У������Ŀ���� ��������Ӧ�����ӷ���ʽ�� ��
��4�����̢��У������ɵ�����J��ʹ����ʯ��ˮ����ǣ�������MnCO3��Ӧ�����ӷ���ʽ��___________��
��5����MnCO3���Ƶ���Ҫ�Ĵ���MnO2��MnCO3 + O2
�� MnO2 + CO2��
O2
�� MnO2 + CO2��
���ڿ����м��� 460.0 g��MnCO3���õ�332.0 g��Ʒ������Ʒ������ֻ��MnO����ò�Ʒ��MnO2������������ ����Ħ������/g����MnCO3 115 MnO2 87 MnO 71��
��1��b d��2��Fe(OH)3��Al(OH)3��3��ʹMnS �� Cu2+���١���ַ�Ӧ��MnS + Cu2+ = Mn2+ + CuS����4��Mn2+ + 2HCO3- = MnCO3 + CO2��+H2O��5��78.6%
��������
�����������1����Fe2+����ΪFe3+��ȥ���ʣ�������Լ�����Ҫ��������������������Լ�ֻ�������ʷ�Ӧ��������ԭ���ʷ�Ӧ����Ӧ���������µ����ʣ��ĸ�ѡ���У�MnO2 ��Ӧ������Ҫ��Mn2+��H2O2��Ӧ������ˮ��˫��ˮ���ȼ����ֽ⣬û�ж������ʣ���bd��ȷ����2������pH��5.2��������֪Fe2+��Al3+����Fe(OH)3��Al(OH)3����״̬���ڣ���3������MnS��Ϊ��ʹ����Cu2+����CuS������ȥ���ʽ���Ŀ����ʹMnS �� Cu2+���١���ַ�Ӧ�����ӷ���ʽMnS + Cu2+ = Mn2+ + CuS������4��������֪Mn2+�ͼ����HCO3-��Ӧ������CO2�����MnCO3�����������ӷ���ʽMn2++2HCO3- =MnCO3
+CO2��+H2O����5��MnCO3���ȷֽ�ΪMnO��MnO��������ΪMnO2����Ʒ��������MnO��460.0 gMnCO3�����ʵ���Ϊ4mol�����Ȳ���4molMnO�������MnO2���ʵ���Ϊxmol������xmolMnO������ʣ��MnOΪ(4-x)mol�������������Ϊ(4-x)mol��71g/mol+xmol��87g/mol=332g��x=3����MnO2����������= =78.6%
=78.6%
���㣺���κ������ε��ת�䣻���ܵ���ʵ��ܽ�ƽ�⣻���ӷ���ʽ����д

 ��У����ϵ�д�
��У����ϵ�д�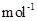 ��MnCO3 115 MnO2 87 MnO 71��
��MnCO3 115 MnO2 87 MnO 71��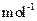 ��MnCO3 115 MnO2 87 MnO 71��
��MnCO3 115 MnO2 87 MnO 71��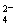
 ��MnCO3 115
MnO2 87 MnO 71��
��MnCO3 115
MnO2 87 MnO 71��