题目内容
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O NH4Cl+NaHCO3(晶体)依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
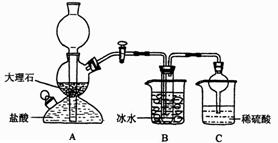
(1)A装置中所发生反应的离子方程式为 。
C装置中稀硫酸的作用为 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)

参照表中数据,请分析B装置中使用冰水是因为 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。现有下列试剂:盐酸、浓氨水、生石灰、蒸馏水,利用本题所提供的试剂(只限一种)及试管、酒精灯等主要仪器,通过简单实验判断该晶体是碳酸氢钠晶体,而不是碳酸氢铵或食盐晶体,简述操作方法、实验现象及结论:
。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
(1)(2分)CaCO3+2H+ Ca2++CO2+H2O;(2分)吸收从B装置中的试管内逸出
的氨气,减少对环境的污染 (2)(2分)温度越低,碳酸氢钠的溶解度越小,便于析出(3)
(1分)A与B(1分)饱和NaHCO3溶液(其他合理答案均可给分)(2分)除去CO2中混
合的HCl气体 (4)(5分)取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还
有白色固体剩余,则晶体不是NH4HCO3;待试管冷却后,向剩余固体中加入适量盐酸,若
反应并产生大量气泡,则晶体是NaHCO3,而不是食盐。(其他合理答案均可给分)(5)(2
分)60%





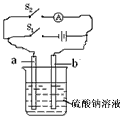
 原理(图中a、b两电极的材料选用多孔碳棒)。
原理(图中a、b两电极的材料选用多孔碳棒)。