题目内容
2. 金属冶炼和处理常涉及氧化还原反应.
金属冶炼和处理常涉及氧化还原反应.(1)由下列物质冶炼相应金属时采用电解法的是BD
A.Fe2O3B.NaCl C.Cu2S D.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2═4CuSO4+2H2O,该反应的还原剂是Cu2S,当1mol O2发生反应时,还原剂所失电子的物质的量为4mol
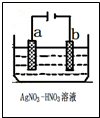
(3)如图为电解精炼银的示意图,a(填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成的该气体为NO2,电极反应为NO3-+e-+2H+=NO2↑+H2O.
分析 (1)电解法:冶炼活泼金属K、Ca、Na、Mg、Al,一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得;热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等);热分解法:Hg、Ag用加热分解氧化物的方法制得,物理分离法:Pt、Au用物理分离的方法制得;
(2)失电子化合价升高的反应物是还原剂,根据得失电子相等计算失去电子的物质的量;
(3)电解精炼银时,粗银作阳极,若b极有少量红棕色气体生成,则b电极上硝酸根离子得电子生成二氧化氮.
解答 解:(1)活泼金属采用电解法冶炼,钠、铝都是活泼金属,采用电解熔融态NaCl、Al2O3的方法冶炼,故答案为:BD;
(2)在该反应中,Cu元素化合价由+1升高到+2,S元素由-2升高到+6,所以Cu2S做还原剂;
氧化还原反应中得失电子数相等,所以当有1molO2参与反应时失去4mol电子,则还原剂所失电子的物质的量为4mol;
故答案为:Cu2S;4;
(3)电解精炼时,粗银做阳极,所以粗银是a极;b电极是阴极,发生还原反应,生成了红棕色气体是NO2,电极反应:NO3-+e-+2H+=NO2↑+H2O,
故答案为:a;NO2,NO3-+e-+2H+=NO2↑+H2O.
点评 本题考查了金属的冶炼方法、氧化还原反应、电解原理等知识点,根据金属的活泼性确定冶炼方法、离子的放电顺序来分析解答,难度不大.

练习册系列答案
相关题目
12.在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,则下列说法正确的是( )
| A. | 锌电极为电流流出 | B. | 锌电极为正极 | ||
| C. | 锌电极有气泡 | D. | 反应中Zn被氧化 |
13.下列是几种原子的基态电子排布,电负性最大的原子是( )
| A. | 1s22s22p63s23p64s2 | B. | 1s22s22p63s23p3 | ||
| C. | 1s22s22p63s23p2 | D. | 1s22s22p4 |
10.某有机物的结构简式如右,它可能发生的反应类型有:①取代;②加成;③消去;④水解;⑤酯化;⑥中和;⑦氧化;⑧加聚.下列正确的是( )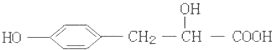
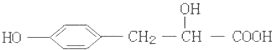
| A. | ①②③⑤⑥⑦ | B. | ②③④⑥⑧ | C. | ①②③④⑥ | D. | ③⑤⑥⑦⑧ |
7.在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强.
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强.
| A. | ①②③④ | B. | ①②④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
14.下列有机物分子中,相邻的五个原子可以构成一个正四面体的是( )
| A. | CHCl3 | B. | CH(CH3) 3 | C. | CCl4 | D. | CH3CH3 |
5.将贮满某种干燥气体的试管倒置于滴有酚酞的水中,轻轻摇晃后,水可以充满试管且溶液变成红色.该气体可能是( )
| A. | NO2 | B. | N2 | C. | SO2 | D. | NH3 |