题目内容
19.有X、Y、Z三种元素,其中X的负一价阴离子的原子核外电子排布与氙的原子核外电子排布相同;Y有两种氧化物,其水溶液都呈碱性.在其氧化物中,相对分子质量分别是62和78.在X和Y化合生成物的水溶液中滴入淡黄绿色的Z单质的水溶液,溶液由无色变成深黄色.Z和X的原子最外层电子数相等.试回答:(1)元素符号:XI,YNa,ZCl.
(2)Y的两种氧化物为Na2O和Na2O2.用化学方程式解释它们的水溶液呈碱性的原因.Na2O+H2O═2NaOH、2Na2O2+2H2O═4NaOH+O2↑
(3)Z的单质溶于水,滴加到X和Y形成的化合物的水溶液中,发生了置换反应反应(填基本反应类型).有关反应的离子方程式为Cl2+2I-═2Cl-+I2.
分析 有X、Y、Z三种元素,其中X的负一价阴离子的原子核外电子排布与氙的原子核外电子排布相同,则X为I元素;
Y有两种氧化物,其水溶液都呈碱性,在其氧化物中,相对分子质量分别是62和78,则Y为Na元素;
在X和Y化合生成物的水溶液中滴入淡黄绿色的Z单质的水溶液,溶液由无色变成深黄色,氯气和碘离子发生置换反应生成碘,Z和X的原子最外层电子数相等,Z为Cl元素;
(1)根据以上分析知,X、Y、Z分别是I、Na、Cl元素;
(2)Y的氧化物有氧化钠和过氧化钠;氧化钠、过氧化钠都和水反应生成NaOH;
(3)Z单质为氯气,X和Y形成的化合物是NaI,氯气具有强氧化性,能氧化碘离子生成碘.
解答 解:有X、Y、Z三种元素,其中X的负一价阴离子的原子核外电子排布与氙的原子核外电子排布相同,则X为I元素;
Y有两种氧化物,其水溶液都呈碱性,在其氧化物中,相对分子质量分别是62和78,则Y为Na元素;
在X和Y化合生成物的水溶液中滴入淡黄绿色的Z单质的水溶液,溶液由无色变成深黄色,氯气和碘离子发生置换反应生成碘,Z和X的原子最外层电子数相等,Z为Cl元素;
(1)根据以上分析知,X、Y、Z分别是I、Na、Cl元素,故答案为:I;Na;Cl;
(2)Y的氧化物有氧化钠和过氧化钠,化学式为Na2O、Na2O2;氧化钠、过氧化钠都和水反应生成NaOH,反应方程式分别为Na2O+H2O═2NaOH、2Na2O2+2H2O═4NaOH+O2↑,导致溶液呈碱性,
故答案为:Na2O;Na2O2;Na2O+H2O═2NaOH、2Na2O2+2H2O═4NaOH+O2↑;
(3)Z单质为氯气,X和Y形成的化合物是NaI,氯气具有强氧化性,能氧化碘离子生成碘,该反应为置换反应,离子方程式为Cl2+2I-═2Cl-+I2,故答案为:置换反应;Cl2+2I-═2Cl-+I2.
点评 本题考查位置结构性质相互关系及应用,侧重考查学生推断及知识运用能力,涉及氧化还原反应、置换反应,正确判断元素是解本题关键,题目难度不大.

 考前必练系列答案
考前必练系列答案| A. | 胶体、溶液、浊液的分类依据是分散质微粒直径大小 | |
| B. | “卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关 | |
| C. | 向1 mol•L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 | |
| D. | 可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体 |
| A. | 某无色溶液中:Al3+、Cu2+、SO42-、Cl- | |
| B. | 由水电离的c(H+)=1×10-12 mol•L-1的溶液中:Fe2+、K+、Cl-、NO3- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:Na+、Mg2+、NO3-、Cl- | |
| D. | 含有大量HCO3-的溶液中:NH4+、Al3+、Ca2+、Cl- |
| A. | 纯净物中一定存在化学键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 只有金属元素和非金属元素化合时才能形成离子键 | |
| D. | 离子化合物中可能含共价键,共价化合物中不含离子键 |
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
2H2(g)+O2(g)=2H2O(l)△H3
常温下取体积为4:1的甲烷和氢气混合气体11.2L(标况),完全燃烧后恢复常温,放出热量为( )
| A. | 0.4△H1+0.05△H3 | B. | 0.4△H1+0.05△H2 | C. | 0.4△H1+0.1△H3 | D. | 0.4△H1+0.2△H3 |
| A. | Li、C、O原子最外层电子数依次增加 | B. | P、S、Cl元素最高正化合价依次升高 | ||
| C. | N、O、F原子半径依次增大 | D. | Li、Na、K的金属性依次增强 |
| A. | 0.8 mol | B. | 0.6 mol | C. | 0.5 mol | D. | 0.2 mol |
| A. | NO:0.06mol•L-1 | B. | H2O:0.002mol•L-1 | ||
| C. | NH3:0.002mol•L-1 | D. | O2:0.00125mol•L-1 |
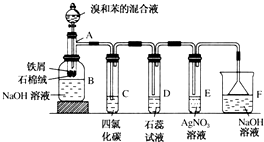 双鸭山市第一中学高二化学兴趣小组设计的苯和液溴反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.
双鸭山市第一中学高二化学兴趣小组设计的苯和液溴反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.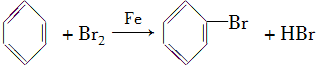 .
.