题目内容
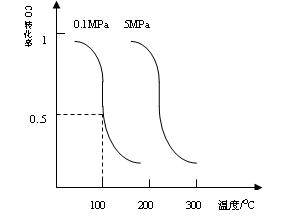
如图所示,将两烧杯用导线如图相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是


| A.Cu极附近OH-浓度增大 |
| B.Cu极为原电池负极 |
| C.电子流向是由C极流向Pt极 |
| D.当C极上有4 mol电子转移时,Pt极上有1 mol O2生成 |
A
正确答案:A
右边原电池,负极Zn―2e-=Zn2+ 正极2H+ +2e-=H2
左边电解池,阴极2H2O+2e-=H2+2OH―,阳极2Cl― ―2e-=Cl2
A 正确;B不正确,Cu极为原电池正极;C.不正确,电子流向是由Zn极流向Cu极
D.不正确,当C极上有4 mol电子转移时,Pt极上有2mol H2生成

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
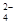


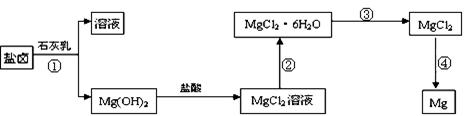
 CH3OH(g)平衡时CO的转化率与温度,压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度,压强的关系如下图: