��Ŀ����
��12�֣�����ͬѧ�������仯��������ʽ���̽����
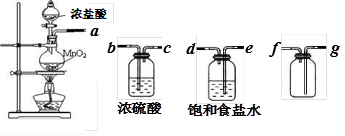
��1��һ��ͬѧ��ͼ1��ʾװ�ö�����Ũ����ķ�Ӧ����ʵ�顣��֪��
2Fe + 6H2SO4(Ũ) Fe2(SO4)3 + 3SO2��+ 6H2O���������̽�����ش�������⡣
Fe2(SO4)3 + 3SO2��+ 6H2O���������̽�����ش�������⡣
�ټ��װ�������Ժ���������м��һ������Ũ���������ƿ��������Ƥ������ʼ��ʱt1ʱ��ʼ���ȣ�����м�����������ݣ����д������ݲ���ʱ�����Ʒ�Ӧ�¶Ȼ������䡣��ͬѧ���ռ��������������ʱ��Ĺ�ϵ���Եر�ʾΪͼ2��
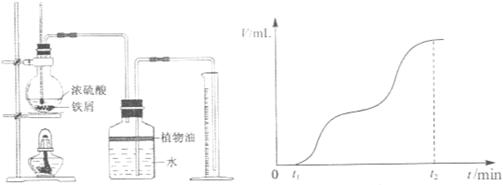
ͼ1 ͼ2
��0��t1ʱ��Σ���м����û���������ɣ�˵������Ũ�����з�����__________��t1��t2ʱ��Σ���Ӧ���ɵ�������__________��
��t2ʱ��ȡ������ӦҺ���ȵμ��������Ʊ�����ˮ��Ȼ��μ�KSCN��Һ������Ѫ��ɫ�����ٵμӹ���������ˮ��ȴ���ֺ�ɫ��ȥ��ͬѧ�ǶԺ�ɫ��ȥ��ԭ��������Եļ��衣��ͬѧ�ļ����ǣ���Һ�е�+3����������Ϊ���ߵļ�̬�������һ�ּ�����__________��Ϊ����֤��ļ��裬�����һ�ּ���ʵ�鷽��__________��
��2����һ��ͬѧ������ϡ����ķ�Ӧ����̽����������a mol Fe�ͺ���b mol HNO3��ϡ�������ʵ�飬��HNO3ֻ����ԭ��NO���ҷ�Ӧ��������Һ�к���Fe3+��Fe2+����a/b��ȡֵ��Χ��__________������Ӧ���������Һ��n(Fe3+):n(Fe2+)=2:1�����ֵΪ__________��
��1��һ��ͬѧ��ͼ1��ʾװ�ö�����Ũ����ķ�Ӧ����ʵ�顣��֪��
2Fe + 6H2SO4(Ũ)
 Fe2(SO4)3 + 3SO2��+ 6H2O���������̽�����ش�������⡣
Fe2(SO4)3 + 3SO2��+ 6H2O���������̽�����ش�������⡣�ټ��װ�������Ժ���������м��һ������Ũ���������ƿ��������Ƥ������ʼ��ʱt1ʱ��ʼ���ȣ�����м�����������ݣ����д������ݲ���ʱ�����Ʒ�Ӧ�¶Ȼ������䡣��ͬѧ���ռ��������������ʱ��Ĺ�ϵ���Եر�ʾΪͼ2��

ͼ1 ͼ2
��0��t1ʱ��Σ���м����û���������ɣ�˵������Ũ�����з�����__________��t1��t2ʱ��Σ���Ӧ���ɵ�������__________��
��t2ʱ��ȡ������ӦҺ���ȵμ��������Ʊ�����ˮ��Ȼ��μ�KSCN��Һ������Ѫ��ɫ�����ٵμӹ���������ˮ��ȴ���ֺ�ɫ��ȥ��ͬѧ�ǶԺ�ɫ��ȥ��ԭ��������Եļ��衣��ͬѧ�ļ����ǣ���Һ�е�+3����������Ϊ���ߵļ�̬�������һ�ּ�����__________��Ϊ����֤��ļ��裬�����һ�ּ���ʵ�鷽��__________��
��2����һ��ͬѧ������ϡ����ķ�Ӧ����̽����������a mol Fe�ͺ���b mol HNO3��ϡ�������ʵ�飬��HNO3ֻ����ԭ��NO���ҷ�Ӧ��������Һ�к���Fe3+��Fe2+����a/b��ȡֵ��Χ��__________������Ӧ���������Һ��n(Fe3+):n(Fe2+)=2:1�����ֵΪ__________��
.(1) �ٶۻ���SO2
�� ��Һ�е�SCN-������������ɫ�����Һ�м�FeCl3,����Һ����ɫ��������
��2�� 1/4 < a/b <3/8 ��9/32
�� ��Һ�е�SCN-������������ɫ�����Һ�м�FeCl3,����Һ����ɫ��������
��2�� 1/4 < a/b <3/8 ��9/32
��1���ٳ���������Ũ�����з����ۻ������Եò������塣�����¶ȵ����ߣ�fie��Ũ������������SO2���塣
����ˮ��ɫ��˵����ˮ����ԭ����˳��������ӻ�ԭ֮�⣬Ҳ�����DZ���Һ�е�SCN-��ԭ��
���Կ���ͨ������SCN-�����𣬼�����ɫ�����Һ�м�FeCl3,����Һ����ɫ����������
��2����������ķ�Ӧ�ķ���ʽ��Fe��4HNO3=Fe(NO3)3��NO����2H2O���������������ʽ��3Fe��8HNO3=3Fe(NO3)2��2NO����4H2O����Ӧ��������Һ�к���Fe3+��Fe2+����a/b��ȡֵ��Χ�� 1/4 < a/b <3/8 ����Ӧ���������Һ��n(Fe3+):n(Fe2+)=2:1�������������������������ֱ���2a/3mol��a/3mol�����Ա���ԭ�������ǣ�b��2a��2a/3��mol�����ݵ��ӵĵ�ʧ�غ��֪��2a/3��3��a/3��2����b��2a��2a/3����3�����a�Ub��9�U32��
����ˮ��ɫ��˵����ˮ����ԭ����˳��������ӻ�ԭ֮�⣬Ҳ�����DZ���Һ�е�SCN-��ԭ��
���Կ���ͨ������SCN-�����𣬼�����ɫ�����Һ�м�FeCl3,����Һ����ɫ����������
��2����������ķ�Ӧ�ķ���ʽ��Fe��4HNO3=Fe(NO3)3��NO����2H2O���������������ʽ��3Fe��8HNO3=3Fe(NO3)2��2NO����4H2O����Ӧ��������Һ�к���Fe3+��Fe2+����a/b��ȡֵ��Χ�� 1/4 < a/b <3/8 ����Ӧ���������Һ��n(Fe3+):n(Fe2+)=2:1�������������������������ֱ���2a/3mol��a/3mol�����Ա���ԭ�������ǣ�b��2a��2a/3��mol�����ݵ��ӵĵ�ʧ�غ��֪��2a/3��3��a/3��2����b��2a��2a/3����3�����a�Ub��9�U32��

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ