��Ŀ����
ij��Ԫ��(��ѧʽ��H2A��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�H2A![]() H++HA- HA-
H++HA- HA-![]() H++A2-
H++A2-
�ش��������⣺
(1)Na2A��Һ��____________(����ԡ������ԡ����ԡ�)��������___________________(�����ӷ���ʽ���Ҫ������˵����ʾ)��
(2)�����£���֪0.1 mol��L-1 NaHA��ҺpH=2����0.1 mol��L-1 H2A��Һ�������ӵ����ʵ���Ũ�ȿ�����______________0.11 mol��L-1(����ڡ������ڡ���С�ڡ�)��������__________________________��
(3)0.1 mol��L-1 NaHA����Һ�и�������Ũ���ɴ�С��˳����____________��
(1)���� A2-+H2O![]() HA-+OH-
HA-+OH-
(2)С�� H2A��һ���������H+��HA-�ĵ������������ã�ʹHA-���ѵ����H+
(3)c(Na+)��c(HA-)��c(H+)��c(A2-)��c(OH-)
������(1)�ɶ�Ԫ��ĵڶ��������ص��֪��Na2A��Һ�ʼ��ԡ�(2)���Ԫ��ĵ�һ�����볹�ף���������������������˵ڶ������룬��ѡ��С�ڡ���(3)��HA-ֻ���ڵ��룬��NaHA��Һ�д���Na+��HA-��A2-��H+��OH-���ʲ����ų����ӵ�Ũ�ȴ�С��ϵ��

(��)�����£���ijһԪ��HA(�ס��ҡ�������������ͬ��һԪ��)��NaOH��Һ�������ϣ�������Һ�����ʵ���Ũ�Ⱥͻ����Һ��pH���±���ʾ��
| ʵ���� | HA�����ʵ��� Ũ��(mol��L-1) | NaOH�����ʵ��� Ũ��(mol��L-1) | ��Ϻ� ��Һ��pH |
| �� | 0.1 | 0.1 | pH=a |
| �� | 0.12 | 0.1 | pH=7 |
| �� | 0.2 | 0.1 | pH>7 |
| �� | 0.1 | 0.1 | pH=10 |
(1)�Ӽ����������������ж�HA��ǿ�ỹ������? �� ��
(2)��������Һ������Ũ��c(A�� )��c(Na+)�Ĵ�С��ϵ�� �� ��
A��ǰ�ߴ� B. ���ߴ� C. ������� D�����ж�
(3)�ӱ���ʵ�����������û����Һ������Ũ���ɴ�С��˳���� �� ��
(4)��������ʵ�����ݣ�д���û����Һ��������ʽ�ľ�ȷ���(��ʽ)��
c(Na+)��c(A-)= �� mol��L-1
(��)ij��Ԫ��(��ѧʽ��H2B��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�
![]()
![]()
�ش��������⣺
(5)��0��1mol��L��Na2B��Һ�У���������Ũ�ȹ�ϵʽ��ȷ���� �� ��
A.c( B2�� )+c(HB�� )=0��1mol��L B��c( B2�� )+ c(HB�� )+c(H2B)=0��1mol��L
C c(OH�� )=c(H+)+ c(HB�� ) D��c(Na+)+c(OH)=c(H+)+ c(HB�� )
(��)�����£���ijһԪ��HA(�ס��ҡ�������������ͬ��һԪ��)��NaOH��Һ�������ϣ�������Һ�����ʵ���Ũ�Ⱥͻ����Һ��pH���±���ʾ��
| ʵ���� | HA�����ʵ��� Ũ��(mol��L-1) | NaOH�����ʵ��� Ũ��(mol��L-1) | ��Ϻ� ��Һ��pH |
| �� | 0.1 | 0.1 | pH=a |
| �� | 0.12 | 0.1 | pH=7 |
| �� | 0.2 | 0.1 | pH>7 |
| �� | 0.1 | 0.1 | pH=10 |
(1)�Ӽ����������������ж�HA��ǿ�ỹ������? �� ��
(2)��������Һ������Ũ��c(A�� )��c(Na+)�Ĵ�С��ϵ�� �� ��
A��ǰ�ߴ� B. ���ߴ� C. ������� D�����ж�
(3)�ӱ���ʵ�����������û����Һ������Ũ���ɴ�С��˳���� �� ��
(4)��������ʵ�����ݣ�д���û����Һ��������ʽ�ľ�ȷ���(��ʽ)��
c(Na+)��c(A-)= �� mol��L-1
(��)ij��Ԫ��(��ѧʽ��H2B��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�
![]()
![]()
�ش��������⣺
(5)��0��1mol��L��Na2B��Һ�У���������Ũ�ȹ�ϵʽ��ȷ���� �� ��
A.c( B2�� )+c(HB�� )=0��1mol��L B��c( B2�� )+ c(HB�� )+c(H2B)=0��1mol��L
C c(OH�� )=c(H+)+ c(HB�� ) D��c(Na+)+c(OH)=c(H+)+ c(HB�� )
 H����A2���ش��������⣺
H����A2���ش��������⣺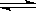 H+ +
A2�� �ش���������:
H+ +
A2�� �ش���������: H++A2-�ش��������⣺
H++A2-�ش��������⣺