题目内容
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)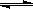 C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
(1)800℃时,0—5min内,以B表示的平均反应速率为
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= ,
该反应为 反应(填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)
(1)0.24mol/( L·min);(2)A、B(2分,)
(3)0.9(mol·L—1)—1(; 吸热 ; (4)向正反应方向。
解析试题分析:(1)在800℃时,当5min 时D的物质的量是0.6mol,根据方程式中B与D的关系可知:消耗B的物质的量是1.2mol,所以0—5min内,以B表示的平均反应速率为V(B)= 1.2mol÷1L÷5min="0.24mol/(" L·min); (2)A.由于该反应是反应前后气体体积不等的反应,所以若容器中压强不变 ,则反应达到平衡,正确; B.由于该反应是反应前后气体体积不等的反应,所以若反应未达到平衡,则任何物质的浓度就会发生变化,所以若混合气体中c(A)不变,反应达到平衡,正确;C.B是反应物,D都是生成物,若反应达到平衡, v正(B)=2v逆(D),现在 2v正(B)=v逆(D),因此反应未达到平衡,错误; D.在任何时刻都存在c(A)=c(C),因此不能判断反应达到平衡,错误。(3)根据已知条件可知:当反应达到平衡时,各种物质的浓度分别是:c(A)=0.4mol/L;c(B)= 1mol/L;c(C)=c(D)=0.6mol/L。所以800℃时的平衡常数K=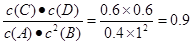 。由于升高温度,D的平衡的物质的量浓度增大,说明升高温度,平衡正向移动,根据平衡移动原理可知,该反应的正反应是吸热反应;(4)在700℃时,根据已知条件可知当反应达到平衡时,各种物质的浓度分别是:c(A)=0.55mol/L;c(B)= 1.3mol/L;c(C)=c(D)=0.45mol/L,在该温度下的化学平衡常数是
。由于升高温度,D的平衡的物质的量浓度增大,说明升高温度,平衡正向移动,根据平衡移动原理可知,该反应的正反应是吸热反应;(4)在700℃时,根据已知条件可知当反应达到平衡时,各种物质的浓度分别是:c(A)=0.55mol/L;c(B)= 1.3mol/L;c(C)=c(D)=0.45mol/L,在该温度下的化学平衡常数是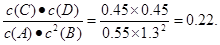 在某一时刻,各种生成物物质的平衡浓度幂之积与各种反应物的浓度的幂之积的比是
在某一时刻,各种生成物物质的平衡浓度幂之积与各种反应物的浓度的幂之积的比是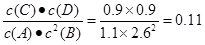 <0.22,所以此时该反应向正反应方向移动。
<0.22,所以此时该反应向正反应方向移动。
考点:考查化学平衡状态的判断、化学反应速率、平衡常数的计算、化学反应进行的方向的判断的知识。

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案下列有关化学反应速率和限度的说法中,不正确的是( )
| A.实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快 |
| B.在金属钠与足量水反应中,增加水的量能加快反应速率 |
C.2SO2+O2 2SO3,反应中,SO2不能全部转化为SO3 2SO3,反应中,SO2不能全部转化为SO3 |
| D.实验室用碳酸钙和盐酸反应抽取CO2,用碳酸钙粉末比块状碳酸钙反应要快 |
可逆反应∶2NO2 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
(10分)800℃、2L密闭容器反应2NO(g)+O2(g) 2NO2(g)体系中, n(NO)随
2NO2(g)体系中, n(NO)随
时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)反应进行到2 s时c (NO)= 。
(2)用O2表示从0~2s内该反应的平均速率υ=___________。
 (3) 反应达到平衡状态时NO的转化率= 。(提示 : )
(3) 反应达到平衡状态时NO的转化率= 。(提示 : )(4)判断一可逆反应是否达到平衡状态的依据有很多,某同学针对该反应提出一种设想:测定容器内气体的密度,当密度不再改变时即可判断出该反应已经达到平衡状态。你认为这种设想是否正确? (填“是”或“否”)请说明你的理由 。
已知:N2O4(g)  2NO2(g) ΔH="+57.20kJ" · mol-1
2NO2(g) ΔH="+57.20kJ" · mol-1
在100℃时,将0.100molN2O4气体充入1L恒容抽空的密闭容器中,每隔一定时间对该容器内的物质浓度进行分析得到下表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4) /mol··L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2) /mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
(1) 该反应的平衡常数表达式为 ______;从表中数据分析:
c1 c2 (填“>” 、“<” 或“="”" )。
(2)下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化
B.NO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗n mol N2O4的同时生成2n mol NO2
E.反应体系中NO2、N2O4的体积比为1:2
(3)若起始时充入NO2气体0.200mol,则达到平衡时NO2气体的转化率为a;其它条件不变时,下列措施能提高NO2转化率的是 (填字母)。
A.降低温度
B.减小NO2的浓度
C.升高温度
D.增加NO2的浓度
E.再充入一定量的He
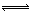 NaNO3(s)+ClNO(g) K1 ?H < 0 (I)
NaNO3(s)+ClNO(g) K1 ?H < 0 (I) Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。 HSO3-+OH-水解平衡的事实是 (填选项字母)。
HSO3-+OH-水解平衡的事实是 (填选项字母)。 C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。
C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。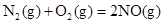
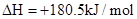
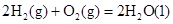
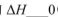 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。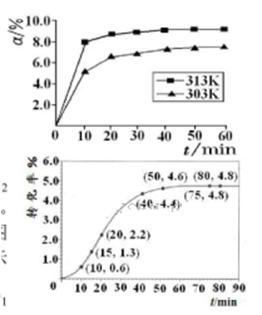
 盐酸与0.2 mol
盐酸与0.2 mol (25℃时,NH3.H2O的电离常数
(25℃时,NH3.H2O的电离常数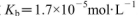 )
)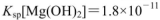 ,
,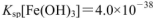 )
)