题目内容
下列叙述中正确的是( )
| A、常温下,浓硫酸可以用铁制容器盛放 | B、SO2具有漂白性,可以使石蕊溶液褪色 | C、硅的化学性质不活泼,在自然界主要以游离态存在 | D、氯气具有强还原性,可以用于自来水的杀菌、消毒 |
分析:A.浓硫酸在常温下可与铁发生钝化反应;
B.二氧化硫不能漂白酸碱指示剂;
C.硅在自然界中以化合态存在;
D.氯气具有强氧化性.
B.二氧化硫不能漂白酸碱指示剂;
C.硅在自然界中以化合态存在;
D.氯气具有强氧化性.
解答:解:A.浓硫酸在常温下可与铁发生钝化反应,使铁在表面生成一层致密的氧化物膜而阻碍反应的进行,可用铁制容器盛放浓硫酸,故A正确;
B.二氧化硫不能漂白酸碱指示剂,可使石蕊试液变红,故B错误;
C.硅为亲氧元素,在自然界中以化合态存在,注意以二氧化硅和硅酸盐的形成存在,故C错误;
D.氯气具有强氧化性,在反应中易得到电子,故D错误.
故选A.
B.二氧化硫不能漂白酸碱指示剂,可使石蕊试液变红,故B错误;
C.硅为亲氧元素,在自然界中以化合态存在,注意以二氧化硅和硅酸盐的形成存在,故C错误;
D.氯气具有强氧化性,在反应中易得到电子,故D错误.
故选A.
点评:本题考查较为综合,涉及浓硫酸、二氧化硫、硅以及氯气的性质,侧重于元素化合物知识的综合理解和运用的考查,为高频考点,难度不大,注意相关基础知识的积累.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
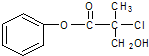 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


