题目内容
11. (1)已知热化学方程式如下:N2(g)+3H2O(1)═2NH3(g)+$\frac{3}{2}$O2(g);△H=+765.2kJ•mol-1,请在坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注.
(1)已知热化学方程式如下:N2(g)+3H2O(1)═2NH3(g)+$\frac{3}{2}$O2(g);△H=+765.2kJ•mol-1,请在坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注.(2)明矾能净水的原因:(用离子方程式和必要的文字解释)明矾溶于水发生Al3++3H2O?Al(OH)3+3H+,生成Al(OH)3胶体能吸附水中的悬浮物质.
(3)已知FeCl3能水解,则配制FeCl3溶液的方法是将FeCl3固体溶解在浓盐酸中,再加水稀释至所需浓度.
(4)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:
铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”)写出铁锅腐蚀负极的电极反应式:2Fe-4e-=2Fe2+
正极的电极反应式:2H2O+O2+4e-=4OH-..
分析 (1)催化剂是通过降低反应的活化能来加快化学反应速率的;
(2)明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附作用,可以净水;
(3)防止铁离子水解,在配制氯化铁溶液时常将FeCl3固体先溶于稀盐酸中,再加水稀释至所需浓度;
(4)中性或弱酸性条件下,钢铁发生吸氧腐蚀;铁、碳和电解质溶液构成原电池,碳作正极,正极上氧气得电子发生还原反应.
解答 解:(1)催化剂是通过降低反应的活化能来加快化学反应速率的,使用催化剂后,活化能降低,图象为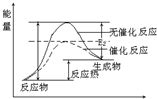 ,故答案为:
,故答案为: ;
;
(2)明矾净水是利用铝离子水解生成氢氧化铝胶体,Al3++3H2O?Al(OH)3+3H+,生成的氢氧化铝胶体具有吸附作用,可以净水
故答案为:明矾溶于水发生Al3++3H2O?Al(OH)3+3H+,生成Al(OH)3胶体能吸附水中的悬浮物质;
(3)FeCl3为强酸弱碱盐,铁离子水解而使其溶液呈酸性,水解离子反应方程式为Fe3++3H2O?Fe(OH)3+3H+,根据方程式知,为防止铁离子水解,在配制氯化铁溶液时常将FeCl3固体先溶于稀盐酸中,氢离子浓度增大,从而抑制铁离子水解,再加水稀释至所需浓度;
故答案为:将FeCl3固体溶解在浓盐酸中,再加水稀释至所需浓度;
(4)弱酸或中性条件下,钢铁发生吸氧腐蚀,负极的电极反应式:2Fe-4e-=2Fe2+,铁、碳和电解质溶液构成原电池,碳作正极,正极上氧气得电子发生还原反应,电极反应式为:2H2O+O2+4e-=4OH-,故答案为:吸氧;2Fe-4e-=2Fe2+;2H2O+O2+4e-=4OH-.
点评 本题考查较为综合,涉及盐类的水解以及金属的电化学腐蚀及电解池原理,明确钢铁所处环境的酸碱性即可确定其电化学腐蚀类型,难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
1.150℃时,碳酸铵完全分解为气态混合物,其密度为相同条件下氢气的( )
| A. | 8倍 | B. | 10倍 | C. | 12倍 | D. | 14倍 |
19.下列所用材料不属于合金的是( )
| A. | 家用的铝窗 | B. | 温度计用的水银 | C. | 铸造用的黄铜 | D. | 建筑用的钢铁 |
6.下列有关维生素C的说法中正确的是( )
| A. | 维生素C难溶于水 | |
| B. | 食品中添加维生素C不利于身体健康 | |
| C. | 维生素C具有还原性 | |
| D. | 含维生素C的食物不宜在高温下烹调 |
3.除去Na2CO3 固体中混有少量NaHCO3的最佳方法是( )
| A. | 加入适量盐酸 | B. | 加入NaOH溶液 | ||
| C. | 置于坩埚中加热 | D. | 配成溶液后通入CO2 |
3. 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
(一)乙酸正丁酯的制备
①在干燥的50mL圆底烧瓶中,加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用10mL的水洗涤.有机层继续用10mL 10% Na2CO3洗涤至中性,再用10mL的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥.
③将干燥后的乙酸正丁酯滤入50mL烧瓶中,常压蒸馏,收集125~127℃的馏分,得11.6g乙酸正丁酯
请回答有关问题.
(1)冷水应该从冷凝管a(填a或b)管口通入.
(2)步骤①中不断从分水器下部分出生成的水的目的是使用分水器分离出水,使平衡正向移动,提高反应产率,步骤①中判断反应终点的依据是分水器中的水层量不再增加.
(3)产品的精制过程步骤②中,第一次水洗的目的是除去乙酸及少量的正丁醇,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是除去产品中含有的乙酸等杂质.
(4)下列关于分液漏斗的使用叙述正确的是D
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.装液时,分液漏斗中液体的总体积不得超过其容积的$\frac{2}{3}$
C.萃取振荡操作应如图所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(5)步骤③的常压蒸馏,需收集126℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是防止因温差过大,冷凝管炸裂
(6)该实验过程中,生成乙酸正丁酯(式量116)的产率是80%.
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
①在干燥的50mL圆底烧瓶中,加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用10mL的水洗涤.有机层继续用10mL 10% Na2CO3洗涤至中性,再用10mL的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥.
③将干燥后的乙酸正丁酯滤入50mL烧瓶中,常压蒸馏,收集125~127℃的馏分,得11.6g乙酸正丁酯
请回答有关问题.
(1)冷水应该从冷凝管a(填a或b)管口通入.
(2)步骤①中不断从分水器下部分出生成的水的目的是使用分水器分离出水,使平衡正向移动,提高反应产率,步骤①中判断反应终点的依据是分水器中的水层量不再增加.
(3)产品的精制过程步骤②中,第一次水洗的目的是除去乙酸及少量的正丁醇,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是除去产品中含有的乙酸等杂质.
(4)下列关于分液漏斗的使用叙述正确的是D
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.装液时,分液漏斗中液体的总体积不得超过其容积的$\frac{2}{3}$
C.萃取振荡操作应如图所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(5)步骤③的常压蒸馏,需收集126℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是防止因温差过大,冷凝管炸裂
(6)该实验过程中,生成乙酸正丁酯(式量116)的产率是80%.
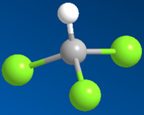 回答下列有机化学问题:
回答下列有机化学问题: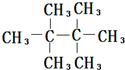 ;
;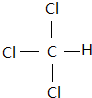 (写出一种).
(写出一种).