题目内容
19.对于可逆反应,2SO2 (g)+O2(g)?2SO3(g)△H<0在一定温度下其平衡数为K,下列说法正确的是( )| A. | 增大SO2的转化率K值一定增大 | B. | 减小压强K值减小 | ||
| C. | K值越大SO2转化率越大 | D. | 升高温度K值增大 |
分析 A、平衡常数是温度的函数,温度不变K不变;
B、平衡常数是温度的函数,压强改变平衡常数不变;
C、平衡常数k越大,说明反应进行的程度越大;
D、正反应是放热反应,升高温度K值减小.
解答 解:A、增大二氧化硫的量,而温度不变,所以K不变,故A错误;
B、压强改变平衡常数不变,故B错误;
C、平衡常数k越大,说明反应进行的程度越大,反应物的转化率越大,故C正确;
D、正反应是放热反应,升高温度K值减小,故D错误;
故选C.
点评 考查平衡常数的意义、化学平衡常数的影响因素等,难度不大,注意化学平衡常数的用途:1、判断反应进行的程度,2、判断反应的热效应,3、判断反应进行的方向,4、计算转化率.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
9.离子化合物①NaCl、②CaO、③NaF、④MgO中,晶格能从小到大顺序正确的是( )
| A. | ①②③④ | B. | ①③②④ | C. | ③①④② | D. | ④②①③ |
10.如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为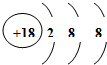 ;
;
(2)地壳中含量最多的金属元素是Al,写出元素⑥③以原子个数比1:1形成化合物的电子式 ;
;
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH;
(4)写出②⑦⑩对应离子还原性由强到弱的次序S2-Cl-F-.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑥ | ② | |||||
| 三 | ③ | ⑤ | ④ | ⑩ | ⑦ | ⑧ | ||
| 四 | ⑨ |
 ;
;(2)地壳中含量最多的金属元素是Al,写出元素⑥③以原子个数比1:1形成化合物的电子式
 ;
;(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH;
(4)写出②⑦⑩对应离子还原性由强到弱的次序S2-Cl-F-.
7. 在一密闭容器中,有下列的可逆反应:A(g)+B(g)?X(g)△H<0,试判断对图4的说法中正确的是(T表示温度,P表示压强)( )
在一密闭容器中,有下列的可逆反应:A(g)+B(g)?X(g)△H<0,试判断对图4的说法中正确的是(T表示温度,P表示压强)( )
 在一密闭容器中,有下列的可逆反应:A(g)+B(g)?X(g)△H<0,试判断对图4的说法中正确的是(T表示温度,P表示压强)( )
在一密闭容器中,有下列的可逆反应:A(g)+B(g)?X(g)△H<0,试判断对图4的说法中正确的是(T表示温度,P表示压强)( )| A. | P3>P4,y轴表示B的转化率 | |
| B. | P3<P4,y轴表示X的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
14.下列关于实验操作的陈述中正确的是( )
| A. | 受热后的蒸发皿要用坩埚钳夹取,并放在石棉网上冷却 | |
| B. | 稀释浓硫酸时,应在量筒中先加入一定量水,再沿器壁缓慢注入浓硫酸,并用玻璃棒搅拌 | |
| C. | 过滤时,为了加速溶液透过滤纸,可以用玻璃棒末端轻轻搅拌滤纸上的混合物 | |
| D. | 不慎将桌面上的酒精灯打翻引起小面积着火时,应迅速用水扑灭火 |
4.下列说法正确的是( )
| A. | 摩尔是七个基本物理量之一,其单位 mol | |
| B. | 1mol任何物质都含有6.02×1023个分子 | |
| C. | 气体的摩尔体积为22.4L | |
| D. | 摩尔质量在数值上等于该物质的相对分子质量或相对原子质量 |
11.下列说法正确的是( )
| A. | 卫生部公告2011年5月1日起全面叫停面粉增白剂,由此可知:应当严格禁止在食品中使用任何食品添加剂 | |
| B. | BaSO4在医学上用作钡餐,Ba2+对人体无毒 | |
| C. | 往稀米粥中加入少量加碘食盐,能检验食盐中是否含碘 | |
| D. | 处理废水时加入明矾作为净水剂可以除去水中悬浮的杂质 |
8.下列反应中,氧化剂与还原剂物质的量的关系不是1:2的是( )
| A. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑ | |
| B. | 3S+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$2K2S+K2SO3+3H2O | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+H2O | |
| D. | O3+2KI+H2O=2KOH+I2+O2 |
5.关于非金属元素N、O、Cl、S的叙述,正确的是( )
| A. | 在通常情况下其单质均为气体 | B. | 其单质均由双原子分子构成 | ||
| C. | 其单质都能跟某些金属单质反应 | D. | 每种元素仅生成一种氢化物 |