题目内容
现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是
| A.加入10mL 0.01mol·L-1的NaOH溶液 |
| B.加入10mL 的水进行稀释 |
| C.加水稀释成100mL |
| D.加入10mL 0.01mol·L-1的盐酸溶液 |
C
解析试题分析:A、强酸完全电离,不存在电离平衡,因此pH=1的某强酸溶液中氢离子浓度是0.1mol/L,与10mL 0.01mol·L-1的NaOH溶液混合后酸过量,反应后溶液中氢离子浓度=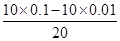 =0.045mol/L,所以溶液的pH不是2,A不正确;B、加入10mL 的水进行稀释后溶液中氢离子的浓度大于0.01mol/L,所以pH不是2,B不正确;C、加水稀释成100mL即稀释10倍后,氢离子的浓度是0.01mol/L,所以溶液的pH=2,C正确;D、加入10mL 0.01mol·L-1的盐酸溶液后氢离子浓度=
=0.045mol/L,所以溶液的pH不是2,A不正确;B、加入10mL 的水进行稀释后溶液中氢离子的浓度大于0.01mol/L,所以pH不是2,B不正确;C、加水稀释成100mL即稀释10倍后,氢离子的浓度是0.01mol/L,所以溶液的pH=2,C正确;D、加入10mL 0.01mol·L-1的盐酸溶液后氢离子浓度=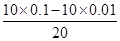 =0.055mol/L,所以溶液的pH不是2,D不正确,答案选C。
=0.055mol/L,所以溶液的pH不是2,D不正确,答案选C。
考点:考查pH的计算

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
下列说法正确的是
| A.KClO3和SO3溶于水后均能导电,故KClO3和SO3都是电解质 |
| B.常温下将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.常温下,等浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| D.25℃时,用pH=3的盐酸滴定等浓度的氨水至溶液的pH=7,V(氨水)<V(盐酸) |
根据下表提供的数据,判断下列离子方程式或化学方程式正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4×10-7 |
| K2=6×10-11 |
A.向Na2CO3溶液中滴加少量氯水:CO32-+2Cl2+H2O=2Cl-+2HClO+CO2↑
B.向NaHCO3溶液中滴加少量氯水:2HCO3-+Cl2=Cl-+ClO-+2CO2↑+H2O
C.向NaClO溶液中通少量CO2:CO2+NaClO+H2O=NaHCO3+HClO
D.向NaClO溶液中通过量CO2:CO2+2NaClO+H2O=Na2CO3+2HClO
下列表述正确的是
| A.0.1mol·L-1Na2CO3溶液中:[OH-]=[HCO3-]+[H+]+[H2CO3] |
| B.0.1mol·L-1CH3COONa溶液中:[Na+]=[CH3COO-]+[OH-] |
| C.CH3COONa、NaOH和Na2CO3三种溶液的pH相同,则浓度大小顺序:c (NaOH) <c (Na2CO3) <c(CH3COONa) |
| D.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至中性,溶液中离子浓度的关系:[CH3COO-]>[Na+]>[OH-]=[H+] |
下列过程或现象与盐类水解无关的是
| A.草木灰不能与铵混合使用态氮肥 |
| B.铁在潮湿的环境下生锈 |
| C.加热氯化铁溶液颜色变深 |
| D.浓硫化钠溶液有臭味 |
下列溶液,一定呈中性的是
| A.c(H+)=1×10-7mol·L-1的溶液 |
| B.c(H+)=c(OH-)=1×10-6mol·L-1的溶液 |
| C.pH=14-pOH的溶液 [注pOH=-lg c(OH-)] |
| D.由等体积、等物质的量浓度的一元酸溶液与NaOH溶液混合后所形成的溶液 |
以下物理量只与温度有关的是
| A.醋酸的电离度 | B.醋酸钠的水解程度 |
| C.水的离子积 | D.氨气的溶解度 |
运用电离常数判断可以发生的反应是
| 酸 | 电离常数(25oC) |
| 碳酸 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| 次溴酸 | Ki=2.4×10-9 |
A.HBrO+Na2CO3→NaBrO+NaHCO3
B.2HBrO+Na2CO3→2NaBrO+H2O+CO2↑
C.HBrO+NaHCO3→NaBrO+H2O+CO2↑
D.NaBrO+CO2+H2O→NaHCO3+HBrO
 H+ + A2-,则下列说法正确的是( )
H+ + A2-,则下列说法正确的是( )