题目内容
已知水的电离方程式:H2O 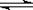 H+ + OH-。下列叙述中,正确的是
H+ + OH-。下列叙述中,正确的是
| A.升高温度,KW增大,pH不变 |
| B.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低 |
| C.向水中加入少量硫酸,c(H+)增大,KW不变 |
| D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低 |
C
解析试题分析:A.升高温度,KW增大,C(H+)增大,溶液 的pH减小。错误。B.向水中加入氨水,由于氨水中的电解质一水合氨会发生电离:NH3?H2O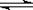 NH4++OH-。增加氢氧根离子的浓度,对水的电离平衡起到了抑制作用。使水的电离平衡向逆向移动。水中的氢离子和氢氧根离子的浓度不再相等,最终 溶液中的c(OH-)比原来大。错误。C. 向水中加入少量硫酸,对水的电离平衡起到了抑制作用,但平衡移动的趋势是很微弱的,最后溶液显酸性。c(H+)增大,由于溶液中的KW只与温度有关。温度不变,Kw就不变。正确。D.向水中加入少量固体CH3COONa, CH3COO-会与水电离产生的氢离子结合成弱电解质CH3COOH,促进了水的电离,使水继续电离直至新的平衡状态。最后由于C(OH-)>C(H+).所以溶液显碱性。错误。
NH4++OH-。增加氢氧根离子的浓度,对水的电离平衡起到了抑制作用。使水的电离平衡向逆向移动。水中的氢离子和氢氧根离子的浓度不再相等,最终 溶液中的c(OH-)比原来大。错误。C. 向水中加入少量硫酸,对水的电离平衡起到了抑制作用,但平衡移动的趋势是很微弱的,最后溶液显酸性。c(H+)增大,由于溶液中的KW只与温度有关。温度不变,Kw就不变。正确。D.向水中加入少量固体CH3COONa, CH3COO-会与水电离产生的氢离子结合成弱电解质CH3COOH,促进了水的电离,使水继续电离直至新的平衡状态。最后由于C(OH-)>C(H+).所以溶液显碱性。错误。
考点:考查温度、外加酸、碱、盐对水的电离平衡、平衡常数、离子浓度等影响的知识。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
下列有关电解质溶液中微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后的溶液中:c(Na+)>c(Cl-) |
| C.已知Ka(HF)=7.2×10-4,Ka(HCN)=6.2×10-10,等体积等浓度的NaF、NaCN溶液中,前者离子总数小于后者 |
| D.浓度均为0.1 mol·L-1的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为:③>②>① |
在一定条件下,Na2CO3溶液中存在CO32-+H2O HCO3-+OH-平衡。下列说法不正确的是( )
HCO3-+OH-平衡。下列说法不正确的是( )
A.稀释溶液,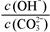 减小 减小 | B.加入NaOH固体,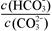 减小 减小 |
| C.升高温度,平衡常数增大 | D.通入CO2,溶液pH减小 |
关于pH相同的醋酸和盐酸,下列叙述正确的是
| A.取等体积的醋酸和盐酸,分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n |
| B.取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸 |
| C.取等体积的两种酸,分别用完全一样的NaOH溶液进行中和,醋酸消耗NaOH的物质的量比盐酸消耗的多 |
| D.两种酸中c (CH3COO-) > c (Cl-) |
25℃时,Fe(OH)3的Ksp=4×10-38,若使某溶液中Fe3+完全沉淀所需pH最接近
| A.3 | B.7 | C.9 | D.11 |
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O 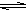 CH3COO- + H3O+ CH3COO- + H3O+ |
B.Br- + H2O 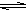 HBr + OH- HBr + OH- |
C.CO32- + 2H2O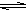 H2CO3 + 2OH- H2CO3 + 2OH- |
D.NH4+ + H2O 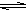 NH3·H2O + H+ NH3·H2O + H+ |
下列溶液中各微粒的浓度关系正确的是
| A.pH=4的盐酸中:c(H+)=4.0mol·L-1 |
| B.NH4Cl溶液中:c(Cl-)=c(NH4+) |
| C.NaCl溶液中:c(Na+) + c(H+)= c(Cl-)+c(OH-) |
| D.NaHCO3溶液中:c(HCO3-)+c(H2CO3)+ c(CO32-) =c(Na+) |
20℃时,有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水 ④pH=11的NaOH溶液。下列说法不正确的是
| A.若将四种溶液稀释100倍,溶液pH的大小顺序:③>④>①>② |
| B.③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③>④ |
| C.①与②混合,所得混合溶液的pH=3 |
| D.②和③混合后,溶液呈碱性 |