题目内容
等物质的量浓度的KCl、MgCl2、AlCl3三种溶液。现欲完全沉淀其中的Cl—,消耗相同物质的量浓度的AgNO3溶液的体积比为3:2:1,则上述三种溶液的体积比为
A 1:1:1 B 6:3:2 C 3:2:1 D 9:3:1
D
解析:

煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
试回答下列问题
(1)上述正向反应是: ▲ 反应(选填:放热、吸热)。
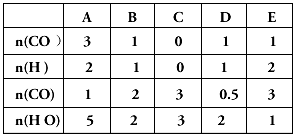
(2)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 ▲ (选填A、B、C、D、E)。
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
(3)已知在一定温度下:C(s)+CO2(g) ![]() 2CO(g)平衡常数K;
2CO(g)平衡常数K;
C(s) + H2O(g) ![]() CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1;
CO(g)+H2O(g)![]() H2(g)+CO2(g) 平衡常数K2 ,
H2(g)+CO2(g) 平衡常数K2 ,
则K、K1、K2之间的关系是: ▲ 。
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020 mol/L,在该条件下,CO的最大转化率为: ▲ 。
(5)若在800℃进行,设起始时CO和H2O(g)共为5mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y= ▲ 。
(6)在VL密闭容器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO燃烧热为283kJ/mol,H2燃烧热为286kJ/mol),则T℃平衡常数K= ▲ 。
| 煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。 已知: 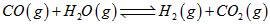 的平衡常数随温度的变化如下表 的平衡常数随温度的变化如下表 | ||||||||
| ||||||||
| 试回答下列问题: (1)上述正向反应是:___________反应(选填:放热、吸热) (2)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 __________(选填A、B、C、D、E) | ||||||||
 | ||||||||
(3)已知在一定温度下: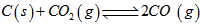 平衡常数K 平衡常数K 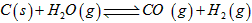 平衡常数K1 平衡常数K1 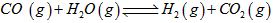 平衡常数K2 平衡常数K2 则K、K1、K2之间的关系是_________________ (4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为: ________________ (5)若在800℃时进行,设起始时CO和H2O共为5mol,水蒸气的体积分数为x,平衡时CO转化率为y,则y随x变化的函数关系式为:y=__________________ (6)在VL密闭器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变)。将混合气体燃烧,测得放出的热量为2842kJ(已知燃烧1molCO放热283KJ,燃烧 1molH2放热为286KJ) 则T℃平衡常数K=_________________ |
 H2(g)+CO2(g)的平衡常数随温度的变化如表:
H2(g)+CO2(g)的平衡常数随温度的变化如表: 2CO(g)平衡常数K;
2CO(g)平衡常数K; CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1; H2(g)+CO2(g) 平衡常数K2,
H2(g)+CO2(g) 平衡常数K2,