题目内容
在容积不变的密闭容器中进行如下反应:N2+3H2 2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
 2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是| A.平衡不发生移动 | B.平衡沿着逆反应方向移动 |
| C.正逆反应速率都增大 | D.NH3的质量分数增加 |
CD
试题分析:将平衡体系中各物质的浓度都增加到原来的2倍,因为体积不变,相当于是增大了二倍压强,正逆反应速率都增大,平衡正向移动,使得氨的质量分数增大,因此选CD。

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
 2SO3(g) + 197 kJ实验测得有关数据如下:
2SO3(g) + 197 kJ实验测得有关数据如下: 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化如图示曲线。下列说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化如图示曲线。下列说法正确的是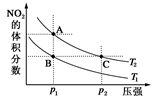
 2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol?L-1,则该反应的平衡常数为( )
2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol?L-1,则该反应的平衡常数为( ) CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示: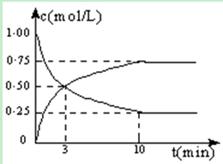
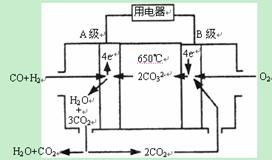
 R(g)+2 L,如图所示R%是R的体积分数,t是时间,下列关于该反应的分析正确的是( )
R(g)+2 L,如图所示R%是R的体积分数,t是时间,下列关于该反应的分析正确的是( )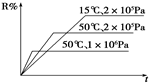
 2NO2 ΔH>0)
2NO2 ΔH>0)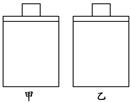
 2HI的平衡体系,加压后密闭体系中的混合气体密度增加
2HI的平衡体系,加压后密闭体系中的混合气体密度增加