题目内容
将NO2、NH3、O2的混合气体26.88L通过稀硫酸后,溶液质量增加45.75g,气体体积缩小为2.24L,将带火星的木条插入其中,木条不复燃.则原混合气体的平均相对分子质量为(气体体积均在标准状况下测定)( )
分析:根据混合气体所发生的反应:氨气与稀硫酸溶液发生反应、NO2和O2在溶液中发生反应结合公式n=
进行计算.
| V |
| Vm |
解答:解:该混合气体的物质的量为n=
=
=1.2mol;氨气与稀硫酸溶液发生如下反应:2NH3+H2SO4=(NH4)2SO4(若氨气过量,则过量的氨气会溶于水);NO2和O2在溶液中发生如下反应:3NO2+H2O=2HNO3+NO;2NO+O2=2NO2;将两个反应方程式相加可得总反应方程式:O2+4NO2+2H2O=4HNO3(此反应仅用于计算)由质量守恒定律可得:溶液增加的质量为溶解的气体的质量,所以溶液增加的质量加剩余气体的质量为原混合气体的质量,带火星的木头不复燃说明氧气充分反应,则剩余的2.24L气体为NO;剩余气体的物质的量为n=
=
=0.1mol,则剩余的NO的质量为m=n×M=0.1mol×30g/mol=3g,所以原混合气体的质量为3g+45.75g=48.75g,所以原混合气体的平均摩尔质量M=
=
=40.625g/mol.
综上所述结合选项,则得出结论:原混合气体的平均相对分子质量为40.625(摩尔质量在数值上等于相对分子质量).
故选D.
| V |
| Vm |
| 26.88L |
| 22.4L/mol |
| V |
| Vm |
| 2.24L |
| 22.4L/mol |
| m |
| n |
| 48.75g |
| 1.2mol |
综上所述结合选项,则得出结论:原混合气体的平均相对分子质量为40.625(摩尔质量在数值上等于相对分子质量).
故选D.
点评:本题是一道平均分子量的计算题,考查学生分析和解决问题的能力,综合性较强,难度较大.

练习册系列答案
相关题目
SCR法(选择性催化还原技术)是一种以NH3作为还原剂,将烟气中NOX分解成无害的N2和H2O的干法脱硝技术,反应原理为:①6NO+4NH3═5N2+6H2O;②6NO2+8NH3═7N2+12H2O;③NO+NO2+2NH3═2N2+3H2O;下列说法正确的是( )
| A、NOX主要来自于汽车尾气的排放,是引起温室效应的主要气体之一 | B、N2中Π键与O键之比为1:2 | C、反应③中每生成22.4LN2,转移电子数1.5NA | D、NH3的沸点比PH3的沸点高 |
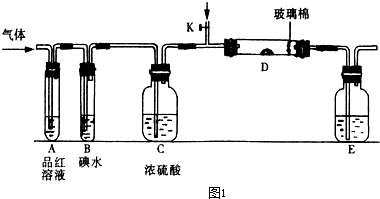
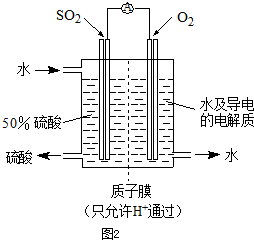
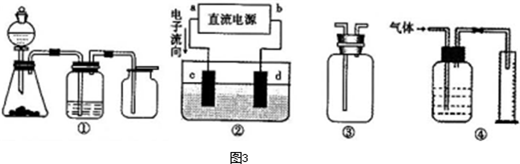
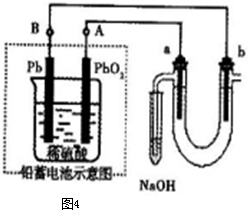
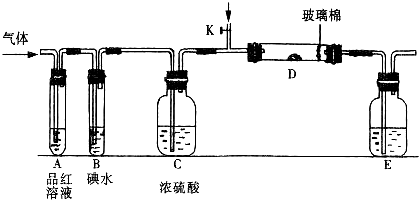
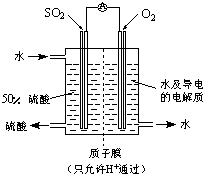
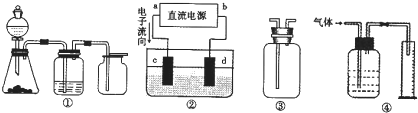
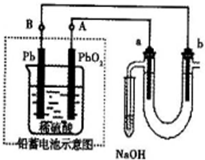
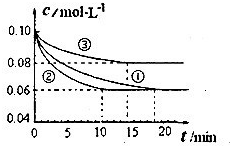 (2013?烟台一模)氮及其化合物在工农业生产中具有重要作用.
(2013?烟台一模)氮及其化合物在工农业生产中具有重要作用.