题目内容
11.元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | 第三周期元素的最高正化合价等于它所处的主族序数 | |
| C. | 短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 | |
| D. | 同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
分析 A、根据周期表中金属性、非金属性的变化规律来考虑;
B、根据同周期元素化合价的变化规律来判断;
C、第一周期元素最多可以排2个电子;
D、根据同族元素的性质的变化规律判断.
解答 解:A、处于金属和非金属分界线的元素既有金属性又有非金属性,如硅元素,故A错误;
B、第三周期的元素从Na到Cl最高化合价从正一价到正七价和族序数相等,故B正确;
C、H元素、Li元素形成离子后达到2电子结构和氦结构相同,不是8电子稳定结构,故C错误;
D、第一主族的所有元素最外层都为一个电子,但是H元素与Na元素性质差异很大,同一主族的元素的原子,最外层电子数相同,化学性质相似,故D错误.
故选B.
点评 本题考查元素周期表和元素周期律,注意把握规律性知识和元素周期表中某些元素的特性,明确元素性质的变化规律即可解答,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
1.下列说法不正确的是( )
| A. | 早在1000多年前,我国就已采用加热胆矾(CuSO4•5H2O)或绿矾(FeSO4•7H2O) 的方法制硫酸,尽管硫酸的生产工艺几经改进,此方法仍然是工业生产硫酸的主要方法 | |
| B. | 氢能是未来能源结构中最具发展潜力的清洁能源之一.目前已有专家已研究出用淀粉或纤维素与水在酶作用下转变为二氧化碳和氢气的方法制氢气.从整个循环来看,利用该方法得到的氢能来源于太阳能 | |
| C. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到,合成A的一种途经是:CH3C≡CH+CO+CH3OH$\stackrel{Pd}{→}$CH2=C(CH3) COOCH3,其过程符合绿色化学的原则 |
2.在一定温度下,向aL恒容密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)?2Z(g).此反应达到平衡的标志是( )
| A. | 容器内X、Y、Z的速率之比为1:2:2 | |
| B. | 单位时间生成0.1 mol X的同时生成0.2 mol Z | |
| C. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| D. | 容器内气体密度不随时间变化 |
19.有一种常见的有机抗冻剂,1mol该有机物与足量金属钠反应,生成的气体在标准状况下的体积为22.4L.该有机物可能是( )
| A. | 甲醇 | B. | 乙醇 | C. | 乙二醇 | D. | 丙三醇 |
6.下列说法中正确的是( )
| A. | 40K与40Ca原子中的中子数相等 | |
| B. | 互为同位素的两种核素,它们原子核内的质子数一定相等 | |
| C. | 人们发现了112种元素,即共有112种核素 | |
| D. | 原子结构模型演变历史可以表示为: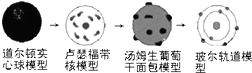 |
1.下列所述事实与化学(离子)方程式不相符的是( )
| A. | 能说明盐酸是强酸:2HCl+CaCO3═CaCl2+CO2↑+H2O | |
| B. | 能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+═2Fe3++2H2O | |
| C. | 能说明NH3结合H+能力比H2O强:NH3+H3O+═NH4++H2O | |
| D. | 能说明CH3COOH是弱电解质:CH3COO-+H2O?CH3COOH+OH- |
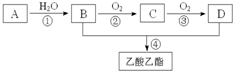 已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国 家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国 家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.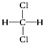 和
和
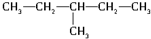 和
和
 =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O