题目内容
下列说法不正确的是( )
| A.硅单质是将太阳能转化为电能的常用材料 |
| B.氯气可用于自来水的杀菌消毒,说明氯气无毒 |
| C.光线透过树叶间的缝隙形成光柱与胶体的性质有关 |
| D.采用原煤脱硫技术,可减少燃煤时产生的SO2 |
B
解析试题分析:硅单质是良好的半导体材料,可以做太阳能电池,A正确;氯气用于自来水消毒是利用氯气溶于水反应生成了次氯酸有强氧化性,但是氯气是有毒气体,B错误;光线透过树叶间的缝隙形成光柱属于丁达尔现象,造成该现象的原因是形成了气溶胶,C正确;煤的燃烧会产生大量的SO2,采用原煤脱硫技术加入CaCO3等物质,可以减少燃煤产生的二氧化硫,D正确;故选择D。
考点:本题考查的是化学与生活的知识。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列操作和现象与结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
下列反应中,调节反应物用量或浓度不会改变反应产物的是 ( )
| A.CO2通入石灰水 | B.硝酸中加入铜片 |
| C.硫酸中加入锌粉 | D.HCl溶液滴入NaHCO3溶液 |
下列分析正确的是
| A.钠久置于空气中,可以和空气中的有关物质反应,最终生成NaHCO3 |
| B.在高温下用氢气还原MgCl2可制取金属镁 |
| C.实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3 COOH>H2CO3 |
| D.氮气的化学性质通常非常稳定,但在放电条件下可以与O2反应生成NO2 |
下列化学物质在实验室存放,方法正确的是
| A.浓硝酸保存在无色试剂瓶中 |
| B.浓硫酸保存在带玻璃塞的广口瓶中 |
| C.少量金属钠保存在煤油中 |
| D.漂白粉可露置在空气中保存 |
将一定质量的Mg、Al合金投入2.0 mol/L、250 mL的稀硫酸中,金属全部溶解。然后向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( )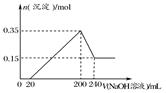
| A.当加入NaOH溶液的体积为20 mL时,溶液的pH等于7 |
| B.当加入NaOH溶液的体积为20 mL时,溶液中的溶质只有硫酸镁和硫酸铝 |
| C.生成的H2在标准状况下的体积为11.2 L |
| D.所加NaOH溶液的物质的量浓度为5.0 mol/L |
下列反应所得溶液中一定只含一种溶质的是 ( )
| A.向NaOH溶液中通入CO2 |
| B.向Ca(OH)2溶液中通入Cl2 |
| C.向蒸馏水中加入少量金属Na |
| D.向Al2(SO4)3溶液中滴入Ba(OH)2溶液 |
X、Y、Z、W四种物质的转化关系如图所示。下列组合中不符合该关系的是( )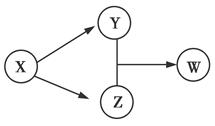
| | A | B | C | D |
| X | HCl | Na2O2 | Na2CO3 | SO2 |
| Y | FeCl2 | NaOH | CO2 | Na2SO3 |
| Z | Cl2 | Na2CO3 | CaCO3 | H2SO4 |
| W | FeCl3 | NaHCO3 | Ca(HCO3)2 | NaHCO3 |
下列化学实验事实的描述及其结论都正确的是( )
| A.将饱和氯水滴到淀粉碘化钾试纸上,试纸先变蓝后变白,说明氯水具有漂白性 |
| B.将SO2通入含HClO的溶液中,生成H2SO4,说明HClO酸性比H2SO4强 |
| C.FeCl3溶液可以腐蚀印刷电路板上的Cu,说明Fe的金属活动性大于Cu |
| D.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝熔点高于铝 |