题目内容
向27.2g Cu和Cu2O(物质的量之比为2︰1)的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2 。在所得溶液中加入1.0 mol/L的NaOH溶液1.0L,此时溶液呈中性,金属离子恰好完全沉淀?下列有关说法错误的是
| A.混合物中Cu的物质的量为0.2 mol |
| B.产生的NO在标准状况下的体积为4.48L |
| C.硝酸的物质的量浓度为2.6mol/L |
| D.Cu?Cu2O与硝酸反应后剩余HNO3为0.2mol |
C
试题分析:A、设Cu2O的物质的量为
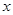 mol,则Cu的物质的量为
mol,则Cu的物质的量为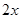 mol,则可得等式:
mol,则可得等式: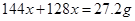 ,解得
,解得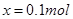 ,则
,则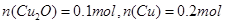 。故选项A正确。
。故选项A正确。B、混合物与稀硝酸反应,生成Cu(NO3)2 的物质的量为0.4mol。转移的电子数为0.6mol,设生成NO的物质的量为
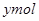 ,则可得关系式:
,则可得关系式: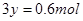 ,解得
,解得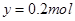 ,因此其在标准状态下的体积
,因此其在标准状态下的体积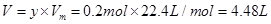 。因此选项B正确。
。因此选项B正确。C、混合物反应生成Cu(NO3)2 的物质的量为0.4mol,需消耗硝酸0.8mol,又反应生成0.2mol的NO,需硝酸0.2mol。因此总共需要硝酸的物质的量为1mol;又混合物与酸反应后硝酸剩余0.2mol,因此整个过程中硝酸的物质的量为
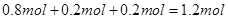 ,其浓度
,其浓度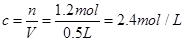 ,故选项C说法错误。
,故选项C说法错误。 D、混合物反应生成Cu(NO3)2 的物质的量为0.4mol,可知与NaOH反应生成的Cu(OH)2的物质的量为0.4mol,需要NaOH的物质的量为0.8mol。而整个反应消耗的NaOH的物质的量为1mol,因此有0.2mol的NaOH与硝酸反应,故选项D正确。综上,答案选C。
点评:金属与硝酸的反应属于中学化学的重点内容,应重点掌握。需注意硝酸无论浓稀均具有氧化性。同时在做此类涉及计算的选择题时,应利用好质量守恒定律。

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
 水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
 将 (填“增大”、 “减小”或“不变”);
将 (填“增大”、 “减小”或“不变”);