��Ŀ����
��6�֣���������(��Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO������)����ȡ���ֹ���Ʒ���������£�
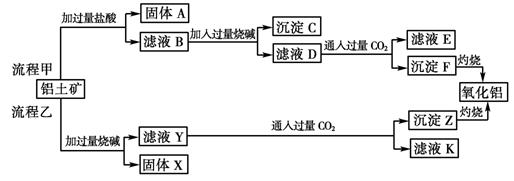
��ش��������⣺
(1)���̼������������Al3�������ӷ���ʽΪ ��
(2)�����Ҽ����ռ������SiO32�������ӷ���ʽΪ ��
(3)��֤��ҺB��Fe3������ȡ������Һ������ (���Լ�����)��
(4)��ҺE��K�����ʵ���Ҫ�ɷ��� (�ѧʽ)��д������Һ��һ����;
��
(5)��֪298 Kʱ��Mg(OH)2���ܶȻ�����Ksp��5.6��10��12��ȡ��������ҺB������һ�������ռ�ﵽ�����ܽ�ƽ�⣬���pH��13.00������¶��²�������Һ�е�c(Mg2��)�� ��
��6�֣�ÿ��1�֣���(1)Al2O3��6H��===2Al3����3H2O
(2)SiO2��2OH��===SiO32����H2O (3)���軯��(�������ᡢ������Һ�Ⱥ�����)
(4)NaHCO3���ƴ���������ͷ۵Ⱥ����� (5)5.6��10��10 mol/L
����������1������������������������ᷴӦ�ķ���ʽ��Al2O3��6H��===2Al3����3H2O��
��2���������������������������������Һ��Ӧ�ķ���ʽ��SiO2��2OH��===SiO��H2O��
��3�����������ӵ��Լ���KSCN��Һ�����DZ��ӡ�
��4������CO2���ǹ����ģ�������Һ�е�������Ҫ����̼�����ƣ�����Ҫ��;���ƴ���������ͷ۵ȡ�
��5��pH��13��������Һ�е�OH��Ũ����0.1mol/L����˸���������þ���ܶȻ�������֪�����¶��²�������Һ�е�c(Mg2��)��5.6��10��12��0.12��5.6��10��10 mol/L��